题目内容
下列说法中正确的是( )
| A、标准状况下,22.4L水中所含的分子数约为6.02×1023 | ||
B、标准状况下,aL的氧气和氮气的混合物中含有的分子数约为
| ||
| C、常温常压下,含NA个O3分子的气体的物质的量小于1 mol | ||
| D、28gCO与16gO2的体积比为1:1 |
考点:物质的量的相关计算
专题:计算题
分析:A.标准状况下,水的状态为液体,不能使用标况下的气体摩尔体积计算其物质的量;
B、根据标况下气体的体积计算出气体的物质的量及含有的分子数;
C、含NA个O3分子的气体的物质的量为1mol,与条件无关;
D、气体的体积与条件有关的.
B、根据标况下气体的体积计算出气体的物质的量及含有的分子数;
C、含NA个O3分子的气体的物质的量为1mol,与条件无关;
D、气体的体积与条件有关的.
解答:
解:A.标准状况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故A错误;
B、标况下,aL氧气和氮气的物质的量为:
mol,含有的分子数约为
mol×6.02×1023,故B正确;
C、含NA个O3分子的气体的物质的量为1mol,故C错误;
D、题目中未指明气体所在的条件,故无法求体积比,故D错误.
故选B.
B、标况下,aL氧气和氮气的物质的量为:
| a |
| 22.4 |
| a |
| 22.4 |
C、含NA个O3分子的气体的物质的量为1mol,故C错误;
D、题目中未指明气体所在的条件,故无法求体积比,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数,注意标准状况下的条件及物质的状态,本题难度不大.

练习册系列答案
相关题目
某一红色粉末可能是Fe2O3、Cu2O其中一种或二者混合物,将粉末放入足量稀硫酸(已知Cu2O+2H+=Cu2++Cu+H2O)中,观察分析该粉末组成下列合理的是( )
| A、若固体完全溶解,则粉末中不可能有Cu2O |
| B、若固体不能完全溶解,则粉末中肯定有Cu2O |
| C、若固体完全溶解,溶液中再加KSCN,变红,则原粉末仅是Fe2O3 |
| D、若固体不能完全溶解,溶液中再加KSCN,不变红,则原粉末仅是Cu2O |
已知氧化性Br2>Fe3+.FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:aFe2++bBr-+cCl2═dFe3++eBr2+fCl-下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A、2 6 4 2 3 8 |
| B、2 4 3 2 2 6 |
| C、2 0 1 2 0 2 |
| D、2 2 2 2 1 4 |
下列实验方案能够达到预期目的是( )
| A、区别苯和乙苯:加酸性高锰酸钾溶液,振荡,观察现象 |
| B、检验无水乙醇中是否含有少量水:加硫酸铜晶体观察现象 |
| C、乙醇的消去反应、皂化反应、淀粉的水解反应均可用浓硫酸作催化剂 |
| D、检验氯代烃中的氯元素时,可先加氢氧化钠溶液加热,再加入硝酸溶液,最后加入硝酸银溶液来进行检验 |
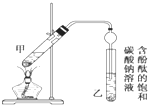 某学生在实验室制取乙酸乙酯的主要步骤如下:
某学生在实验室制取乙酸乙酯的主要步骤如下: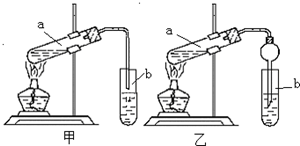 某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题:
某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题: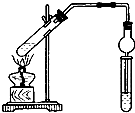 用如图所示实验装置制取乙酸乙酯.回答以下问题:
用如图所示实验装置制取乙酸乙酯.回答以下问题: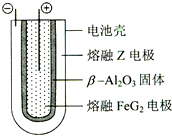 有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空:
有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空: