题目内容
8.国际上至今发现具有巨磁电阻效应的20多种金属纳米多层膜中,其中三种是我国学者发现的,Mn和Bi形成的晶体薄膜是一种金属间化合物(晶胞结构如图),有关说法正确的是( )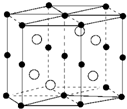
| A. | 锰价电子排布为3d74s0 | B. | Bi是d区金属 | ||
| C. | 该晶体的化学式为MnBi | D. | 该合金堆积方式是简单立方 |
分析 A.Mn为25号元素,其3d、4s电子为其价电子,3d能级有5个电子、4s能级有2个电子;
B.Bi最后排入的电子为p电子;
C.根据原子半径知,黑色小球表示Mn原子、白色小球表示Bi原子,根据均摊法计算原子个数,从而确定化学式;
D.简单立方为六面体.
解答 解:A.Mn为25号元素,其3d、4s电子为其价电子,3d能级有5个电子、4s能级有2个电子,锰价电子排布为3d54s2,故A错误;
B.Bi最后排入的电子为p电子,所以Bi位于p区,故B错误;
C.根据原子半径知,黑色小球表示Mn原子、白色小球表示Bi原子,Bi原子数目为6,Mn原子数目为1+2×$\frac{1}{2}$+12×$\frac{1}{6}$+6×$\frac{1}{3}$=6,故该晶体物质的化学式MnBi,故C正确;
D.简单立方为六面体,根据图知,该合金堆积方式不是简单立方,故D错误;
故选C.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、元素周期表结构、原子核外电子排布、原子堆积方式等知识点,侧重考查学生分析判断及对知识的综合应用,棱上原子被几个晶胞共用是易错点.

练习册系列答案
相关题目
19.化学与科学、社会、环境、生活等都密切相关,下列有关说法错误的是( )
| A. | 食品包装中的干燥剂必须用特别包装纸包装,其成分多为氧化钙颗粒,也有硅胶颗粒 | |
| B. | 蛋白质、塑料、合成橡胶、光导纤维都是高分子化合物 | |
| C. | Fe2O3、CuO、PbO等金属氧化物是我国古代就已经使用的用于烧碱釉陶的彩色釉面原料 | |
| D. | 控制汽车尾气、工业尾气、建筑扬尘、垃圾焚烧等的任意排放是治理雾霾天气重要环节 |
16.在冰晶石(Na3[AlF6])晶胞中,[AlF6]3-占据的位置相当于NaCl晶胞中Cl-占据的位置,则冰晶石晶胞中含有的原子数与NaCl晶胞中含有的原子数之比为( )
| A. | 2:1 | B. | 3:2 | C. | 5:2 | D. | 5:1 |
13.某元素原子核外M层电子数是L层电子数的一半,则此元素是( )
| A. | Li | B. | C | C. | Si | D. | S |
18.银氨溶液可用于检测CO气体,实验室研究的装置如图:
(1)甲酸(HCOOH)遇浓硫酸分解生成CO和H2O,该反应体现浓硫酸的脱水性性.
(2)装置A中软管的作用是恒压,使甲酸溶液能顺利滴下.
(3)为验证上层清液中产物的成分,进行如下实验:
a.测得上层清液pH为10.
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体.
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象.
①实验c的目的是对比试验,排除银氨溶液对产物检验的干扰.
②根据上述实验现象判断,上层清液中产物成分为(NH4)2CO3(填化学式).
(4)设计实验证明黑色固体的成分是Ag:可供选择的试剂有:浓硫酸、浓硝酸、NaOH溶液、NaCl溶液.
取少量上述黑色固体,用蒸馏水洗净,滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl溶液,能产生白色沉淀,说明黑色固体是Ag单质.(补充必要的实验内容及实验现象)
(5)从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2.
①写出生成AgCl沉淀的离子反应[Ag(NH3)2]++OH-+3H++Cl-=AgCl↓+2NH4++H2O.
②若该反应中消耗3.3g羟氨,理论上可得银的质量为10.8g.
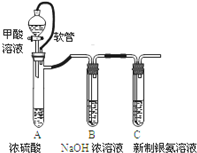 | 已知:①银氨溶液的化学式为: Ag(NH3)2OH ②反应结束后试管C底部有黑色 沉淀生成, ③分离出上层清液和底部黑色 固体备用. |
(2)装置A中软管的作用是恒压,使甲酸溶液能顺利滴下.
(3)为验证上层清液中产物的成分,进行如下实验:
a.测得上层清液pH为10.
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体.
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象.
①实验c的目的是对比试验,排除银氨溶液对产物检验的干扰.
②根据上述实验现象判断,上层清液中产物成分为(NH4)2CO3(填化学式).
(4)设计实验证明黑色固体的成分是Ag:可供选择的试剂有:浓硫酸、浓硝酸、NaOH溶液、NaCl溶液.
取少量上述黑色固体,用蒸馏水洗净,滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl溶液,能产生白色沉淀,说明黑色固体是Ag单质.(补充必要的实验内容及实验现象)
(5)从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2.
①写出生成AgCl沉淀的离子反应[Ag(NH3)2]++OH-+3H++Cl-=AgCl↓+2NH4++H2O.
②若该反应中消耗3.3g羟氨,理论上可得银的质量为10.8g.