题目内容
镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取.主要步骤如下:

(1)为了使MgCl2转化为Mg(OH)2,试剂①可以选用 .试剂②可以选用 .
(2)验证MgCl2已完全转化为Mg(OH)2的方法是 .
(3)由MgCl2溶液得到无水MgCl2的方法是 .

(1)为了使MgCl2转化为Mg(OH)2,试剂①可以选用
(2)验证MgCl2已完全转化为Mg(OH)2的方法是
(3)由MgCl2溶液得到无水MgCl2的方法是
考点:海水资源及其综合利用
专题:实验设计题
分析:向海水中加入NaOH或Ca(OH)2,NaOH或Ca(OH)2和硫酸镁反应生成Mg(OH)2沉淀,然后过滤得到Mg(OH)2和滤液,将Mg(OH)2溶于稀盐酸中得到MgCl2,将MgCl2溶液在HCl氛围中蒸干得到MgCl2,电解熔融MgCl2得到Mg单质,
(1)将为了使MgCl2转化为Mg(OH)2,应该先加入碱使镁离子转化为氢氧化镁沉淀,然后用酸溶解;
(2)向滤液中加入碱液,观察是否有白色沉淀生成;
(3)将MgCl2溶液在HCl氛围中蒸干得到MgCl2.
(1)将为了使MgCl2转化为Mg(OH)2,应该先加入碱使镁离子转化为氢氧化镁沉淀,然后用酸溶解;
(2)向滤液中加入碱液,观察是否有白色沉淀生成;
(3)将MgCl2溶液在HCl氛围中蒸干得到MgCl2.
解答:
解:向海水中加入NaOH或Ca(OH)2,NaOH或Ca(OH)2和硫酸镁反应生成Mg(OH)2沉淀,然后过滤得到Mg(OH)2和滤液,将Mg(OH)2溶于稀盐酸中得到MgCl2,将MgCl2溶液在HCl氛围中蒸干得到MgCl2,电解熔融MgCl2得到Mg单质,
(1)将为了使MgCl2转化为Mg(OH)2,应该先加入碱使镁离子转化为氢氧化镁沉淀,然后用酸溶解,所以试剂①可以选用NaOH或Ca(OH)2 ,试剂②可以选用稀盐酸,故答案为:NaOH或Ca(OH)2 ;稀盐酸;
(2)向滤液中加入碱液,观察是否有白色沉淀生成,其检验方法是取上层清液,滴入Ca(OH)2溶液,若不产生沉淀则证明MgCl2已完全转化为Mg(OH)2,故答案为:取上层清液,滴入Ca(OH)2溶液,若不产生沉淀则证明MgCl2已完全转化为Mg(OH)2;
(3)氯化镁是强酸弱碱盐,在蒸干氯化镁溶液过程中氯化镁水解生成氢氧化镁和HCl,升高温度促进稀盐酸挥发,最终得不到氯化镁,为防止氯化镁水解,将MgCl2溶液在HCl氛围中蒸干得到MgCl2,其操作方法是在不断通入HCl气体的条件下加热蒸发,
故答案为:在不断通入HCl气体的条件下加热蒸发.
(1)将为了使MgCl2转化为Mg(OH)2,应该先加入碱使镁离子转化为氢氧化镁沉淀,然后用酸溶解,所以试剂①可以选用NaOH或Ca(OH)2 ,试剂②可以选用稀盐酸,故答案为:NaOH或Ca(OH)2 ;稀盐酸;
(2)向滤液中加入碱液,观察是否有白色沉淀生成,其检验方法是取上层清液,滴入Ca(OH)2溶液,若不产生沉淀则证明MgCl2已完全转化为Mg(OH)2,故答案为:取上层清液,滴入Ca(OH)2溶液,若不产生沉淀则证明MgCl2已完全转化为Mg(OH)2;
(3)氯化镁是强酸弱碱盐,在蒸干氯化镁溶液过程中氯化镁水解生成氢氧化镁和HCl,升高温度促进稀盐酸挥发,最终得不到氯化镁,为防止氯化镁水解,将MgCl2溶液在HCl氛围中蒸干得到MgCl2,其操作方法是在不断通入HCl气体的条件下加热蒸发,
故答案为:在不断通入HCl气体的条件下加热蒸发.
点评:本题考查海水资源的综合利用,侧重考查学生实验操作、分析能力,明确流程图中每一步发生的反应、基本实验操作是解本题关键,注意从氯化镁溶液中得到氯化镁晶体的方法,题目难度不大.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
化学药品包装瓶上常有一些警示标志.下列化学药品名称与警示标志对应正确的是( )
A、 甲烷 |
B、 浓硫酸 |
C、 汽油 |
D、 烧碱 |
下列说法错误的是( )
| A、用煤制取甲醚(CH3OCH3)替代石油,可以缓解我国石油的供需矛盾 |
| B、医疗上用的“钡餐”其成分是氯化钡 |
| C、氮化硅陶瓷、通讯光缆等都是新型无机非金属材料 |
| D、利用风能、生物能发电,将火力发电用煤进行脱硫处理,有利于环保 |
生产、生活中化学无处不在.下列说法不正确的是( )
| A、大量排放SO2是造成温室效应的主要原因 |
| B、明矾和硫酸铁都常用于净水 |
| C、考古时常用14C测定文物的年代 |
D、 如图是运输浓硝酸的槽罐车上贴的危险警告标签 |
物质的量浓度相同的三种酸HX、HY、HZ的溶液,其pH依次为4、5、6,则KX、KY、KZ的碱性由强到弱的顺序是( )
| A、KX、KZ、KY |
| B、KX、KY、KZ |
| C、KZ、KY、KX |
| D、KY、KZ、KX |
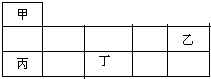 短周期金属元素甲~丁在元素周期表中的相对位置如图所示:下列判断正确的是( )
短周期金属元素甲~丁在元素周期表中的相对位置如图所示:下列判断正确的是( )| A、原子半径:丙>丁>乙 |
| B、单质的还原性:丁>丙>甲 |
| C、甲、乙、丙的氧化物均为共价化合物 |
| D、乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
下列反应中,属于取代反应的是( )
①CH3CH═CH2+Br2
CH3CHBrCH2Br
②C6H6+HNO3
C6H5NO2+H2O
③CH3CH2OH
CH2═CH2↑+H2O
④CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O.
①CH3CH═CH2+Br2
| CCl4 |
②C6H6+HNO3
| 浓H2SO4 |
| △ |
③CH3CH2OH
| 浓H2SO4 |
| △ |
④CH3COOH+CH3CH2OH
| 浓H2SO4 |
| △ |
| A、①② | B、③④ | C、①③ | D、②④ |
下表中列出了25℃、101kPa时一些物质的燃烧热数据
已知键能:C-H键:413.4kJ/mol、H-H键:436.0kJ/mol.则下列叙述正确的是( )
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/kJ/mol | 890.3 | 1299.6 | 285.8 |
| A、2H2(g)+O2(g)=2H2O(g)△H=-571.6 kJ/mol |
| B、C-H键键长小于H-H键 |
| C、C≡C键能为796.0 kJ/mol |
| D、2CH4(g)=C2H2(g)+3H2(g)△H=-376.4 kJ/mol |