题目内容
CH3COOH与NaCl混合溶液中的质子守恒等式是 .
考点:离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:溶液中的质子守恒就是水电离出来的氢离子的浓度等于水电离出来的氢氧根离子的浓度,等式为:氢氧根离子的浓度等于氢离子的浓度加上氢离子的去向,氢离子包括溶液中剩余的氢离子和醋酸根离子水解结合的氢离子,据此进行解答.
解答:
解:溶液中的质子守恒就是水电离出来的氢离子的浓度等于水电离出来的氢氧根离子的浓度,
醋酸为弱电解质,在溶液中部分电离出氢离子:CH3COOH?CH3COO-+H+,溶液中氢离子来自水的电离和醋酸的电离,
所以CH3COOH与NaCl混合溶液中的质子守恒等式为:c(H+)=c(OH-)+c(CH3COO-),
故答案为:c(H+)=c(OH-)+c(CH3COO-).
醋酸为弱电解质,在溶液中部分电离出氢离子:CH3COOH?CH3COO-+H+,溶液中氢离子来自水的电离和醋酸的电离,
所以CH3COOH与NaCl混合溶液中的质子守恒等式为:c(H+)=c(OH-)+c(CH3COO-),
故答案为:c(H+)=c(OH-)+c(CH3COO-).
点评:本题考查了混合液中离子浓度大小比较,题目难度中等,明确质子守恒的含义为解答关键,注意电荷守恒、物料守恒、质子守恒的含义及应用方法.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列电子式正确的是( )
A、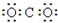 |
B、 |
C、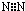 |
D、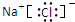 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
①将1mol氯气通入一定量水中发生反应转移电子数为NA
②12.0g熔融的NaHSO4中含有的阳离子数为0.1NA
③在标准状况下,22.4L辛烷中的分子数为NA
④1mol羟基中含有的电子数为10NA
⑤1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA.
①将1mol氯气通入一定量水中发生反应转移电子数为NA
②12.0g熔融的NaHSO4中含有的阳离子数为0.1NA
③在标准状况下,22.4L辛烷中的分子数为NA
④1mol羟基中含有的电子数为10NA
⑤1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA.
| A、②⑤ | B、④⑤ |
| C、①③⑤ | D、③④⑤ |
 在密闭容器中,对于可逆反应A+3B?2C(g),平衡时物质C的体积分数与温度、压强的关系如图所示,下列判断正确的是( )
在密闭容器中,对于可逆反应A+3B?2C(g),平衡时物质C的体积分数与温度、压强的关系如图所示,下列判断正确的是( )| A、A一定为气体,B一定为固体或液体 |
| B、B一定为气体,A一定为固体或液体 |
| C、若正反应的△H<0,则T1<T2 |
| D、若正反应的△H<0,则T1>T2 |
某溶液中由水电离产生的c(OHˉ)=1×10-14 mol?L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
| A、Al3+、Na+、NO3ˉ、Clˉ |
| B、K+、Na+、Clˉ、NO3ˉ |
| C、K+、Na+、Clˉ、AlO2ˉ |
| D、K+、NH4+、SO32ˉ、NO3ˉ |
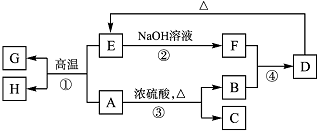 已知A、B、C、D、E、F、G、H可以发生如下图所示的转化(反应过程中部分产物已略去).其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物.
已知A、B、C、D、E、F、G、H可以发生如下图所示的转化(反应过程中部分产物已略去).其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物.