题目内容
20.铬是人体必需的微量元素,但正六价的铬有很强的毒性,人体需要的是三价铬.用肼(N2H4)--氧气燃料电池做电源,以铁做阳极,利用电解法除去污水中的Cr2O72-离子,若污水中含0.2mol的Cr2O72-离子,则标准状况下需消耗N2H4的体积为6.72L.分析 无论酸性还是碱性肼(N2H4)--氧气燃料电池中,负极上都是肼失电子发生氧化反应生成N2,1mol肼反应失去4mol电子;
以铁做阳极,利用电解法除去污水中的Cr2O72-离子发生的离子方程式为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,串联电路中转移电子相等,根据转移电子相等计算消耗肼的体积.
解答 解:无论酸性还是碱性肼(N2H4)--氧气燃料电池中,负极上都是肼失电子发生氧化反应生成N2,1mol肼反应失去4mol电子;
以铁做阳极,利用电解法除去污水中的Cr2O72-离子发生的离子方程式为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,串联电路中转移电子相等,根据转移电子相等得消耗肼的体积=$\frac{0.2mol×(6-3)×2}{4}$×22.4L/mol=6.72L,
故答案为:6.72L.
点评 本题考查电解原理,为高频考点,侧重考查学生分析计算能力,明确各个电极上发生的反应是解本题关键,注意转移电子守恒的灵活运用,题目难度不大.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
11.已知有浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )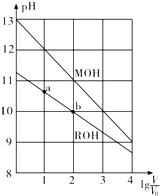

| A. | MOH的碱性强于ROH的碱性 | |
| B. | ROH的电离程度:b点大于a点 | |
| C. | 当1g$\frac{V}{{V}_{0}}$=2时,若两溶液同时升温,则$\frac{c({M}^{+})}{c({R}^{+})}$增大 | |
| D. | 若两溶液无限稀释,则它们的c(OH-)相等 |
15.下列各对物质中,互为同系物的是( )
| A. | CH3-CH═CH2与  | B. |  与 与 | ||
| C. | HCOOC2H5与CH3COOCH3 | D. |  与 与 |
5.下列各组物质中,肯定互为同系物的是( )
| A. | C2H6 C3H8 | B. | CH3COOH CH3COOCH3 | ||
| C. | C3H4 C4H6 | D. |  |
9.短周期主族元素A、B、C、D,原子序数依次增大.A、C的原子序数之差为8,A、B、C三种元素原子的最外层电子数之和为15,且B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A. | 原子半径:A<B<C<D | |
| B. | 最高价氧化物对应水化物的酸性:D<C | |
| C. | 非金属性:A>C | |
| D. | 单质B常温下能溶于浓硝酸 |
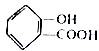
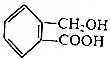 互为同系物
互为同系物 ,请写出将
,请写出将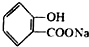 的化学方程式
的化学方程式
 .(提示:环丁烷
.(提示:环丁烷 可简写成□)
可简写成□)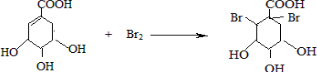 .
. ),其反应类型是消去反应.
),其反应类型是消去反应. 中任意一种.
中任意一种.