题目内容
生产、生活离不开各种化学物质,下列说法不正确的是( )
| A、氧化铝可以用来制造耐火坩埚、耐火管和耐高温的实验仪器 |
| B、潜水艇在紧急情况下可用过氧化钠供氧 |
| C、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| D、工业上常用硅制造光导纤维 |
考点:镁、铝的重要化合物,氯、溴、碘及其化合物的综合应用,硅和二氧化硅,钠的重要化合物
专题:化学应用
分析:A.氧化铝熔点很高,可以做耐火材料;
B.过氧化钠能与二氧化碳反应生成氧气;
C.氯气与碱反应生成次氯酸盐,次氯酸盐进一步转化为次氯酸,具有强氧化性,起杀菌消毒作用;
D.工业上常用二氧化硅制造光导纤维.
B.过氧化钠能与二氧化碳反应生成氧气;
C.氯气与碱反应生成次氯酸盐,次氯酸盐进一步转化为次氯酸,具有强氧化性,起杀菌消毒作用;
D.工业上常用二氧化硅制造光导纤维.
解答:
解:A.氧化铝熔点很高,可以做耐火材料,故A正确;
B.过氧化钠能与二氧化碳反应生成氧气,可以作为供氧剂提供氧气,故B正确;
C、氯气和烧碱反应得到次氯酸钠溶液,水解生成次氯酸具有消毒作用,氯气和石灰乳反应生成的次氯酸钙是漂白粉的有效成分,会生成次氯酸具有杀菌消毒作用,故C正确;
D.工业上常用二氧化硅制造光导纤维,故D错误;
故选D.
B.过氧化钠能与二氧化碳反应生成氧气,可以作为供氧剂提供氧气,故B正确;
C、氯气和烧碱反应得到次氯酸钠溶液,水解生成次氯酸具有消毒作用,氯气和石灰乳反应生成的次氯酸钙是漂白粉的有效成分,会生成次氯酸具有杀菌消毒作用,故C正确;
D.工业上常用二氧化硅制造光导纤维,故D错误;
故选D.
点评:本题考查钠、铝、氯元素化合物的性质以及金属的防护等,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
某无色溶液中只可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO32-、⑥SO42-中的若干种(忽略水电离出的H+、OH-),依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
下列结论正确的是( )
下列结论正确的是( )
| 步骤 | 操 作 | 现 象 |
| (1) | 取少许溶液向其中滴加稀盐酸 | 有气泡产生 |
| (2) | 另取少许溶液向其中滴加氯水,及CCl4振荡,静置 | CCl4层呈橙色 |
| (3) | 向(2)所得水溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| (4) | 将(3)过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
| A、肯定含有的离子是③④⑤ |
| B、肯定没有的离子是②⑤ |
| C、可能含有的离子是①⑥ |
| D、不能确定的离子是③⑥ |
浓盐酸与次氯酸钙能发生反应Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质是( )
①CO2 ②HCl ③H2O(g) ④O2.
①CO2 ②HCl ③H2O(g) ④O2.
| A、①②③④ | B、②③④ |
| C、②③ | D、①④ |
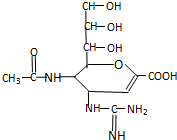 已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性.其分子结构如图:下列说法正确的是( )
已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性.其分子结构如图:下列说法正确的是( )| A、该物质的分子式为C12H19N4O7 |
| B、在一定条件下,该物质可以发生消去、加成、取代等反应 |
| C、1mol该物质与NaOH溶液反应,可以消耗4molNaOH |
| D、该物质能使溴水或高锰酸钾溶液褪色,能与FeCl3溶液发生显色反应 |
下列过程中,最终的白色沉淀不一定是BaSO4的是( )
A、Fe(NO3)2
| ||||||
B、Ba(NO3)2溶液
| ||||||
C、无色溶液
| ||||||
D、无色溶液
|
下列物质是生活中常见的物质,属于强电解质的是( )
| A、干冰 |
| B、BaSO4 |
| C、醋酸 |
| D、酒精 |
25℃时,某强酸溶液pH=a,强碱溶液pH=b,且a+b=13,酸碱溶液混合后溶液的pH=7,则酸溶液的体积(V1)与碱溶液的体积(V2)的关系是( )
| A、V1=10V2 |
| B、V1=2V2 |
| C、V2=10V1 |
| D、V2=2 V1 |