题目内容
W、X、Y、Z、M、Q均为除稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的4倍,Z与M的最低负化合价相同,X、M在周期表中位置如图所示.
(1)X在周期表中的位置为 ,Q的元素名称为 ;
(2)Z与W形成的4核离子的电子式为 ;
(3)由W、Y、Z、M组成的离子化合物在溶液中相互反应的离子方程式为: .
(4)W2与Z2反应化合物甲,W2与Q2反应生成化合物乙.已知反应:
乙(g)+Z2(g)→甲(g)+Q2(g),每生成1mol Q2放热57.8kJ.写出该反应的热化学方程式: ;
(5)X、Y可分别与Z以原子个数比1:1形成化合物丙和丁.在催化剂存在条件下,丙与丁发生可逆反应,生成单质Y2和另一种化合物戊.写出该反应的化学方程式: ;
(6)将1mol丙气体和1mol丁气体充入一装有催化剂的恒压容器中,充分反应达平衡后:
若气体体积较原来减少23%,则丁的转化率为 .
| X | ||
| M |
(2)Z与W形成的4核离子的电子式为
(3)由W、Y、Z、M组成的离子化合物在溶液中相互反应的离子方程式为:
(4)W2与Z2反应化合物甲,W2与Q2反应生成化合物乙.已知反应:
乙(g)+Z2(g)→甲(g)+Q2(g),每生成1mol Q2放热57.8kJ.写出该反应的热化学方程式:
(5)X、Y可分别与Z以原子个数比1:1形成化合物丙和丁.在催化剂存在条件下,丙与丁发生可逆反应,生成单质Y2和另一种化合物戊.写出该反应的化学方程式:
(6)将1mol丙气体和1mol丁气体充入一装有催化剂的恒压容器中,充分反应达平衡后:
若气体体积较原来减少23%,则丁的转化率为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:W、X、Y、Z、M、Q均为除稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的4倍,由于最外层电子数不大于8,则W最外层电子数是1,其原子序数最小,为Li或H元素;X原子最外层电子数为4,Z与M的最低负化合价相同,则Z和M位于同一主族,由原子序数结合元素在周期表中的位置知,X位于第二周期,M位于第三周期,结合原子序数可知,X为碳元素,M为S元素,故Z为O元素;Y的原子序数介于C、O之间,故Y为N元素;Q的原子序数最大,故Q为Cl元素,(2)中Z与W形成的4核离子,则W是H元素,结合物质结构性质解答.
解答:
解:W、X、Y、Z、M、Q均为除稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的4倍,由于最外层电子数不大于8,则W最外层电子数是1,其原子序数最小,为Li或H元素;X原子最外层电子数为4,Z与M的最低负化合价相同,则Z和M位于同一主族,由原子序数结合元素在周期表中的位置知,X位于第二周期,M位于第三周期,结合原子序数可知,X为碳元素,M为S元素,故Z为O元素;Y的原子序数介于C、O之间,故Y为N元素;Q的原子序数最大,故Q为Cl元素,(2)中Z与W形成的4核离子,则W是H元素,
(1)X是C元素,位于第二周期第IVA族,Q是氯元素,故答案为:第二周期第IVA族;氯;
(2)Z与W形成的4核离子为水和氢离子,其电子式为 ,故答案为:
,故答案为: ;
;
(3)由H、N、O、S组成的离子化合物在溶液中相互反应,为亚硫酸铵(或亚硫酸氢铵)与硫酸氢铵反应的,离子方程式为:SO32-+2H+=SO2↑+H2O,故答案为:SO32-+2H+=SO2↑+H2O;
(4)H2与O2反应化合物甲为H2O,H2与Cl2反应生成化合物乙为HCl,故已知反应为:4HCl(g)+O2(g)=2H2O(g)+2Cl2(g),每生成1mol Cl2放热57.8kJ,该反应的热化学方程式:4HCl(g)+O2(g)=2H2O(g)+2Cl2(g)△H=-115.6kJ/mol,
故答案为:4HCl(g)+O2(g)=2H2O(g)+2Cl2(g)△H=-115.6kJ/mol;
(4)C、N可分别与O以原子个数比1:1形成化合物丙和丁分别为CO、NO,在催化剂存在条件下,丙与丁发生反应,生成单质N2和另一种化合物戊,戊为CO2,该反应的化学方程式:2CO+2NO
N2+2CO2,
故答案为:2CO+2NO
N2+2CO2;
(5)令参加反应的NO为xmol,则:
2 CO+2 NO
N2+2 CO2
开始(mol):1 1 0 0
转化(mol):x x 0.5x x
平衡(mol):1-x 1-x 0.5x x
则:(1-x)mol+(1-x)mol+0.5xmol+xmol=(1+1)mol×(1-23)%,
解得x=0.92
故NO的转化率=
×100%=92%
故答案为:92%.
(1)X是C元素,位于第二周期第IVA族,Q是氯元素,故答案为:第二周期第IVA族;氯;
(2)Z与W形成的4核离子为水和氢离子,其电子式为
 ,故答案为:
,故答案为: ;
;(3)由H、N、O、S组成的离子化合物在溶液中相互反应,为亚硫酸铵(或亚硫酸氢铵)与硫酸氢铵反应的,离子方程式为:SO32-+2H+=SO2↑+H2O,故答案为:SO32-+2H+=SO2↑+H2O;
(4)H2与O2反应化合物甲为H2O,H2与Cl2反应生成化合物乙为HCl,故已知反应为:4HCl(g)+O2(g)=2H2O(g)+2Cl2(g),每生成1mol Cl2放热57.8kJ,该反应的热化学方程式:4HCl(g)+O2(g)=2H2O(g)+2Cl2(g)△H=-115.6kJ/mol,
故答案为:4HCl(g)+O2(g)=2H2O(g)+2Cl2(g)△H=-115.6kJ/mol;
(4)C、N可分别与O以原子个数比1:1形成化合物丙和丁分别为CO、NO,在催化剂存在条件下,丙与丁发生反应,生成单质N2和另一种化合物戊,戊为CO2,该反应的化学方程式:2CO+2NO
| ||
故答案为:2CO+2NO
| ||
(5)令参加反应的NO为xmol,则:
2 CO+2 NO
| ||
开始(mol):1 1 0 0
转化(mol):x x 0.5x x
平衡(mol):1-x 1-x 0.5x x
则:(1-x)mol+(1-x)mol+0.5xmol+xmol=(1+1)mol×(1-23)%,
解得x=0.92
故NO的转化率=
| 0.92mol |
| 1mol |
故答案为:92%.
点评:本题考查结构性质位置关系、无机物推断、热化学方程式、化学平衡计算等,推断元素是解题关键,注意根据(2)中的问题确定W元素,需要学生具备扎实的基础,难度中等.

练习册系列答案
相关题目
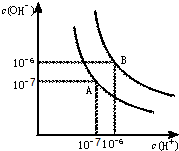 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示.