题目内容
已知环戊烯结构简式为: 可简写为:
可简写为:
降冰片烯的分子结构可表示为:
(1)降冰片烯属于
A.环烃 B.不饱和烃 C.烷烃 D.芳香烃
(2)降冰片烯的分子式为 ;
(3)降冰片烯不具有的性质
A.能溶于水 B.发生氧化反应 C.加成反应 D.常温常压下为气体
(4)写出环戊烯在一定条件下加聚反应方程式: .
 可简写为:
可简写为:
降冰片烯的分子结构可表示为:

(1)降冰片烯属于
A.环烃 B.不饱和烃 C.烷烃 D.芳香烃
(2)降冰片烯的分子式为
(3)降冰片烯不具有的性质
A.能溶于水 B.发生氧化反应 C.加成反应 D.常温常压下为气体
(4)写出环戊烯在一定条件下加聚反应方程式:
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可确定有机物式,有机物含有碳碳双键,可发生加成、加聚和氧化反应,以此解答该题.
解答:
解:(1)由结构简式可知有机物含有环状结构,并含有碳碳双键,则属于环烃和不饱和烃,故答案为:A、B;
(2)由有机物结构简式可知有机物分子式为C7H10,故答案为:C7H10;
(3)分子中含有碳碳双键,可发生加成、氧化反应,烃类物质都不溶于水,且碳原子数大于4,常温下为液体,故答案为:A.D;
(4)碳碳双键能发生加聚反应,则化学反应方程式为 ,故答案为:
,故答案为: .
.
(2)由有机物结构简式可知有机物分子式为C7H10,故答案为:C7H10;
(3)分子中含有碳碳双键,可发生加成、氧化反应,烃类物质都不溶于水,且碳原子数大于4,常温下为液体,故答案为:A.D;
(4)碳碳双键能发生加聚反应,则化学反应方程式为
 ,故答案为:
,故答案为: .
.
点评:本题考查有机物的合成及有机物的性质,明确有机物的结构与性质的关系即可解答,注意把握烯烃的性质来解答,题目难度不大.

练习册系列答案
相关题目
在10L密闭容器中进行如下反应:A(g)+B(g)?2C(g),2分钟后,B由2mol减少到1.2mol,则用单位内A的浓度变化表示的反应速率(VA)是( )
| A、0.02mol/(L?min) |
| B、0.04mol/(L?min) |
| C、0.08mol/(L?min) |
| D、0.8mol/(L?min) |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、16gO2中含有的氧分子数为NA |
| B、1mol镁原子中含有的电子数为NA |
| C、常温常压下,11.2L H2中含有的氢分子数为0.5NA |
| D、1L 1mol/L BaCl2溶液中含有的钡离子数为NA |

 无机化合物可根据其组成和性质进行分类.
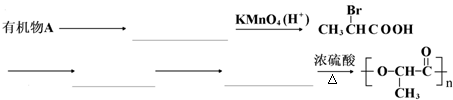
无机化合物可根据其组成和性质进行分类.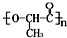 是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋.请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)
是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋.请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)