题目内容
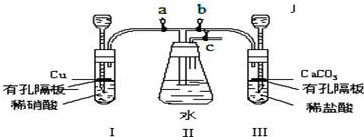
某小组同学用如图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:

(1)将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①氯元素在周期表中的位置为 .
②A中反应的离子方程式: .
③E中氢氧化钠溶液的作用 .
在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论为:
④实验Ⅰ推出的相应结论是否合理?若不合理,请说明理由(若合理,无需填写) .
⑤实验Ⅱ推出相应的结论是否合理?若不合理,请说明理由(若合理,无需填写) .
(2)将B、D、E相连,在B中装浓硝酸和铜片,可制得NO2.B中反应的化学方程式 .

(1)将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①氯元素在周期表中的位置为
②A中反应的离子方程式:
③E中氢氧化钠溶液的作用
在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论为:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
⑤实验Ⅱ推出相应的结论是否合理?若不合理,请说明理由(若合理,无需填写)
(2)将B、D、E相连,在B中装浓硝酸和铜片,可制得NO2.B中反应的化学方程式
考点:探究氯水、氯气的漂白作用,氯气的实验室制法
专题:
分析:(1)①依据氯为17号元素,氯原子中质子数为17,有三个电子层解答;
②二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水;
③氯气有毒,直接排放会污染空气,氯气能够与氢氧化钠溶液反应;
④要验证氯气与水反应的产物具有漂白性应首先排除干燥氯气的影响,需要进行对比实验;
⑤实验室制得的氯气中有杂质气体水蒸气和氯化氢气体,盐酸能和碳酸氢钠反应产生二氧化碳气体;
(2)铜和浓硝酸反应生成的是二氧化氮气、硝酸铜和水.
②二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水;
③氯气有毒,直接排放会污染空气,氯气能够与氢氧化钠溶液反应;
④要验证氯气与水反应的产物具有漂白性应首先排除干燥氯气的影响,需要进行对比实验;
⑤实验室制得的氯气中有杂质气体水蒸气和氯化氢气体,盐酸能和碳酸氢钠反应产生二氧化碳气体;
(2)铜和浓硝酸反应生成的是二氧化氮气、硝酸铜和水.
解答:
解:(1)①氯为17号元素,在周期表中的位置为第三周期第ⅦA族,故答案为:第三周期第ⅦA族;
②二氧化锰与浓盐酸反应生成氯气、氯化锰和水,反应的离子方程式为:MnO2+4H++2Cl-
Mn2++2H2O+Cl2↑,故答案为:MnO2+4H++2Cl-
Mn2++2H2O+Cl2↑;
③氯气有毒,直接排放能污染空气,氯气能与氢氧化钠溶液反应,所以多余的氯气应该用氢氧化钠溶液吸收,故答案为:吸收多余的Cl2;
④没有事先证明干燥的氯气无漂白性,则不能证明氯气与水反应的产物是否具有漂白性,故答案为:不合理;没有事先证明干燥的氯气无漂白性;
⑤氯化氢易挥发,实验室制得的氯气中有杂质气体水蒸气和氯化氢气体,盐酸也能和碳酸氢钠反应产生二氧化碳气体,不一定是氯气与水反应的产物的酸性,故不合理;
故答案为:不合理,制取的氯气中含HCl气体,其溶于水能与NaHCO3粉末反应产生气泡;
(2)铜和浓硝酸反应生成的是二氧化氮气、硝酸铜和水,化学方程式为:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,故答案为:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O.
②二氧化锰与浓盐酸反应生成氯气、氯化锰和水,反应的离子方程式为:MnO2+4H++2Cl-
| ||
| ||
③氯气有毒,直接排放能污染空气,氯气能与氢氧化钠溶液反应,所以多余的氯气应该用氢氧化钠溶液吸收,故答案为:吸收多余的Cl2;
④没有事先证明干燥的氯气无漂白性,则不能证明氯气与水反应的产物是否具有漂白性,故答案为:不合理;没有事先证明干燥的氯气无漂白性;
⑤氯化氢易挥发,实验室制得的氯气中有杂质气体水蒸气和氯化氢气体,盐酸也能和碳酸氢钠反应产生二氧化碳气体,不一定是氯气与水反应的产物的酸性,故不合理;
故答案为:不合理,制取的氯气中含HCl气体,其溶于水能与NaHCO3粉末反应产生气泡;
(2)铜和浓硝酸反应生成的是二氧化氮气、硝酸铜和水,化学方程式为:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,故答案为:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O.
点评:本题考查了氯气的实验室制法、氯气的化学性质,明确实验室制取氯气的反应原理及氯气的化学性质是解题关键,侧重考查学生对实验方案的评价,题目难度中等.

练习册系列答案
相关题目
步行街口的烧烤摊常常买一些腌制类食品如:火腿、香肠等,其实在这里面一般都加了防腐剂,指( )
| A、苯甲酸钠 | B、亚硝酸钠 |
| C、味精 | D、胭脂红 |
已知室温时,0.1mol/L某一元酸HA,PH=4,下列说法正确的是( )
| A、HA在水中有0.001%发生电离 |
| B、HA的电离平衡常数K=10-8mol/L |
| C、升高温度时,PH增大 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列有机物不是同一种物质的是( )
A、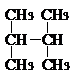 与 与 |
B、 与新戊烷 与新戊烷 |
C、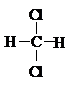 与 与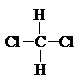 |
| D、C(CH3)3C(CH3)3与CH3(CH2)3C(CH3)3 |