题目内容
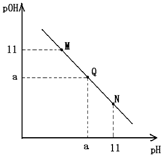 常温下,向一定体积的1mol.L-1的醋酸溶液中逐滴加入等浓度的氢氧化钠溶液,溶液中pOH和pH的变化如图所示,已知该条件下醋酸的电离程度为0.4%,则下列说法不正确的是( )
常温下,向一定体积的1mol.L-1的醋酸溶液中逐滴加入等浓度的氢氧化钠溶液,溶液中pOH和pH的变化如图所示,已知该条件下醋酸的电离程度为0.4%,则下列说法不正确的是( )| A、a为7 |
| B、Q点的水的电离程度在整条曲线中最大 |
| C、M和Q之间(不含Q)的溶液离子浓度排序都满足c(CH3COO-)>c(Na+) |
| D、三点所代表的溶液导电能力,N最大,M最小 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.Q点pOH=pH,溶液显示中性,常温下溶液的pH=7;
B.Q点溶液为中性溶液,当醋酸与氢氧化钠溶液恰好反应生成醋酸钠溶液时,醋酸根离子水解,水的电离程度最大;
C.M和Q之间溶液显示酸性,c(OH-)<c(H+),根据电荷守恒判断c(CH3COO-)、c(Na+)的大小;
D.M点主要为醋酸溶液,醋酸为弱电解质,溶液中离子浓度较小,随着氢氧化钠溶液的加入,生成的醋酸钠为强电解质,溶液中离子浓度逐渐增大,溶液导电性逐渐增强.
B.Q点溶液为中性溶液,当醋酸与氢氧化钠溶液恰好反应生成醋酸钠溶液时,醋酸根离子水解,水的电离程度最大;
C.M和Q之间溶液显示酸性,c(OH-)<c(H+),根据电荷守恒判断c(CH3COO-)、c(Na+)的大小;
D.M点主要为醋酸溶液,醋酸为弱电解质,溶液中离子浓度较小,随着氢氧化钠溶液的加入,生成的醋酸钠为强电解质,溶液中离子浓度逐渐增大,溶液导电性逐渐增强.
解答:
解:A.根据图象可知,Q点时pOH=pH,溶液呈中性,在常温下溶液的pH=7,即a=7,故A正确;
B.酸或碱溶液抑制了水的电离,醋酸根离子水解能够促进水的电离,所以当醋酸与氢氧化钠溶液恰好反应生成醋酸钠溶液时,水的电离程度最大,此时溶液显示碱性,溶液的pH>7,故B错误;
C.M和Q点之间,由于溶液显示酸性,则溶液中一定满足c(OH-)<c(H+),根据电荷守恒c(OH-)+c(CH3COO-)=c(Na+)+c(H+),可知:c(CH3COO-)>c(Na+),故C正确;
D.根据图象可知,M点主要为醋酸溶液,醋酸为弱酸,溶液中离子浓度较小,溶液导电性较弱,随着氢氧化钠溶液的加入,溶液中强电解质醋酸钠的浓度逐渐增大,溶液的导电性逐渐增强,所以溶液导电性在M点最小,在N点最大,故D正确;
故选B.
B.酸或碱溶液抑制了水的电离,醋酸根离子水解能够促进水的电离,所以当醋酸与氢氧化钠溶液恰好反应生成醋酸钠溶液时,水的电离程度最大,此时溶液显示碱性,溶液的pH>7,故B错误;
C.M和Q点之间,由于溶液显示酸性,则溶液中一定满足c(OH-)<c(H+),根据电荷守恒c(OH-)+c(CH3COO-)=c(Na+)+c(H+),可知:c(CH3COO-)>c(Na+),故C正确;
D.根据图象可知,M点主要为醋酸溶液,醋酸为弱酸,溶液中离子浓度较小,溶液导电性较弱,随着氢氧化钠溶液的加入,溶液中强电解质醋酸钠的浓度逐渐增大,溶液的导电性逐渐增强,所以溶液导电性在M点最小,在N点最大,故D正确;
故选B.
点评:本题考查了溶液酸碱性与溶液pH的计算、离子浓度大小比较,题目难度中等,注意掌握溶液酸碱性与溶液pH的关系,明确判断溶液中各离子浓度大小的方法,能够利用电荷守恒、盐的水解原理判断溶液中离子浓度关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有机物命名正确的是( )
A、1,3,4-三甲苯 |
B、α-氨基苯丙酸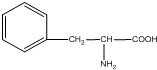 |
| C、2-甲基丙烯 (CH3)2C=CH2 |
| D、2,2-二甲基-3-丁醇 (CH3)3C-CHOH-CH3 |
下列关于化学反应的速率和限度的说法正确的是( )
| A、化学反应速率通常只能用反应物浓度的减少量表示 |
| B、化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| C、影响化学反应速率的条件并不只是温度和催化剂 |
| D、催化剂都能加快化学反应速率,并提高原料利用率或转化率 |
下列化学用语书写正确的是( )
| A、SO2气体通入到溴水中:SO2+Br2+2H2O=4H++SO42-+2Br- |
| B、碳酸钡溶液醋酸:BaCO3+2H+=Ba2++H2O+CO2↑ |
| C、硫氢化钠水解:HS-+H2O=H3O++S2- |
| D、明矾溶液中加入过量的氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
已知w g物质A在O2中充分燃烧后,产物被足量的Na2O2完全吸收后,Na2O2固体增重w g,当A为H2或CO时,上述说法成立.据此推断A不可能是下列物质中的( )
| A、H2和CO的混合气 |
| B、D2 |
| C、甲醇 |
| D、乙醇 |
在pH=3的FeCl3溶液和pH=3的盐酸中,由水电离出来的H+的浓度分别为C1、C2,pH=11的Na2CO3溶液中水电离出来的OH-的浓度为C3,则它们之间的关系是( )
| A、C1<C2<C3 |
| B、C1=C3>C2 |
| C、C1>C2>C3 |
| D、无法判断 |
下列说法正确的是( )
| A、pH=2和pH=1的硝酸中c(H+)之比为10:1 | ||
| B、一元酸与一元碱恰好完全反应后的溶液中一定存在c(H+)=c(OH-) | ||
C、KAl(SO4)2溶液中离子浓度的大小顺序为c(SO
| ||
| D、常温下,将pH均为12的氨水和NaOH溶液分别加水稀释100倍后,NaOH溶液的pH较大 |
下列各化合物的命名中不正确的是( )
| A、CH2=CH-CH=CH2 1,3-丁二烯 |
B、 3-丁醇 3-丁醇 |
C、 邻-甲基苯酚 邻-甲基苯酚 |
D、 2-甲基丁烷 2-甲基丁烷 |
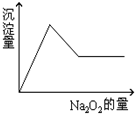 有一透明溶液,可能含有Al3+、Fe3+、K+、Mg2+和Cu2+等离子中的一种或几种.现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀.如加入Na2O2的量与生成白色沉淀的量之间的关系用图来表示.
有一透明溶液,可能含有Al3+、Fe3+、K+、Mg2+和Cu2+等离子中的一种或几种.现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀.如加入Na2O2的量与生成白色沉淀的量之间的关系用图来表示.