题目内容
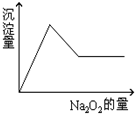 有一透明溶液,可能含有Al3+、Fe3+、K+、Mg2+和Cu2+等离子中的一种或几种.现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀.如加入Na2O2的量与生成白色沉淀的量之间的关系用图来表示.
有一透明溶液,可能含有Al3+、Fe3+、K+、Mg2+和Cu2+等离子中的一种或几种.现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀.如加入Na2O2的量与生成白色沉淀的量之间的关系用图来表示.试推断:原溶液中一定含有
考点:常见离子的检验方法
专题:物质检验鉴别题
分析:根据实验现象判断Fe3+、Cu2+是否存在,根据图象判断Mg2+、Al3+是否存在,根据焰色反应判断K+的存在.
解答:
解:加入Na2O2粉末,过氧化钠与水反应,2Na2O2+2H2O=4NaOH+O2↑,并同时析出白色沉淀,故可推断不含有铁离子和铜离子;
当加入过量的过氧化钠时,先生成白色沉淀,后沉淀部分溶解,推断一定有Mg2+、Al3+,可能含有K+;
K+的检验:用洁净的铂丝蘸取待测液,在酒精灯上灼烧,透过蓝色钴玻璃观察火焰的颜色,火焰呈紫色,说明含有K+;
故答案为:Al3+、Mg2+;Fe3+、Cu2+;K+;用洁净的铂丝蘸取待测液,在酒精灯上灼烧,透过蓝色钴玻璃观察火焰的颜色;火焰呈紫色.
当加入过量的过氧化钠时,先生成白色沉淀,后沉淀部分溶解,推断一定有Mg2+、Al3+,可能含有K+;
K+的检验:用洁净的铂丝蘸取待测液,在酒精灯上灼烧,透过蓝色钴玻璃观察火焰的颜色,火焰呈紫色,说明含有K+;
故答案为:Al3+、Mg2+;Fe3+、Cu2+;K+;用洁净的铂丝蘸取待测液,在酒精灯上灼烧,透过蓝色钴玻璃观察火焰的颜色;火焰呈紫色.
点评:本题考查的是常见阳离子的检验,注意各个离子的性质,结合图象的方式考查增加了难度,本题综合性很强,难度中等.

练习册系列答案
相关题目
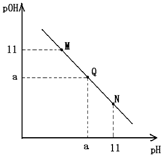 常温下,向一定体积的1mol.L-1的醋酸溶液中逐滴加入等浓度的氢氧化钠溶液,溶液中pOH和pH的变化如图所示,已知该条件下醋酸的电离程度为0.4%,则下列说法不正确的是( )
常温下,向一定体积的1mol.L-1的醋酸溶液中逐滴加入等浓度的氢氧化钠溶液,溶液中pOH和pH的变化如图所示,已知该条件下醋酸的电离程度为0.4%,则下列说法不正确的是( )| A、a为7 |
| B、Q点的水的电离程度在整条曲线中最大 |
| C、M和Q之间(不含Q)的溶液离子浓度排序都满足c(CH3COO-)>c(Na+) |
| D、三点所代表的溶液导电能力,N最大,M最小 |
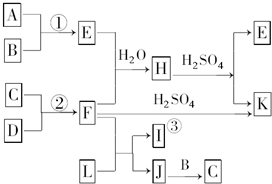
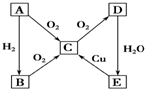 在通常状况下,A为固态单质.根据图转化关系,回答:
在通常状况下,A为固态单质.根据图转化关系,回答: