题目内容
7.在溶液中能共存,加入H+能放出气体的是( )| A. | Ag+ H+ NO3- Cl- | B. | Ca2+ NO3- HCO3- Cl- | ||
| C. | K+ H+ Cl- SO42- | D. | Ca2+ Cl-SO42- CO32- |
分析 A.银离子与氯离子反应生成氯化银沉淀;
B.四种离子之间不反应,加入氢离子后生成二氧化碳气体;
C.四种离子之间不反应,但加入氢离子后不会生成气体;
D.钙离子与硫酸根离子、碳酸根离子反应.
解答 解:A.Ag+、Cl-之间反应生成氯化银沉淀,在溶液中不能大量共存,故A错误;
B.Ca2+、NO3-、HCO3-、Cl-之间不反应,能够共存,加入氢离子后能够生成二氧化碳气体,故B正确;
C.K+、H+、Cl-、SO42-之间不反应,能够共存,但是加入氢离子后不会生成气体,故C错误;
D.Ca2+与SO42-、CO32-之间发生反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.原电池是将化学能转变为电能的装置.关于如图所示原电池的说法不正确的是( )
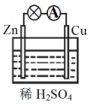

| A. | Zn为负极,Cu为正极 | B. | 电子由锌片通过导线流向铜片 | ||
| C. | 正极反应式为Cu-2e-Cu2+ | D. | 原电池的反应本质是氧化还原反应 |
12. 化学反应中的能量变化,通常主要表现为热量的变化.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.测定中和热的实验装置如图所示:
化学反应中的能量变化,通常主要表现为热量的变化.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.测定中和热的实验装置如图所示:
(1)该图中有两处仪器未画出,它们是泡沫塑料板(硬纸板)、环形玻璃搅拌棒.
(2)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式为(中和热数值为57.3kJ/mol)$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol.
(3)取55mLNaOH溶液和25mL硫酸溶液进行实验,实验数据如表.
近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm2,中和后生成溶液的比热容c=4.08J/(g•℃).则中和热△H=-52.2kJ/mol(取小数点后一位).
(4)有关中和热测定实验,下列说法错误的是bc
a.用温度计测定NaOH溶液起始温度后马上直接测定H2SO4溶液的温度会导致中和热数值比57.3低
b.温度计的冲洗液应倒入小烧杯参与反应
c.混合硫酸和氢氧化钠溶液时应分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.若装置完全相同,操作均没失误,取110mLNaOH溶液和50mL硫酸溶液进行实验,误差比55mLNaOH溶液和25mL硫酸溶液进行实验误差小.
 化学反应中的能量变化,通常主要表现为热量的变化.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.测定中和热的实验装置如图所示:
化学反应中的能量变化,通常主要表现为热量的变化.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.测定中和热的实验装置如图所示:(1)该图中有两处仪器未画出,它们是泡沫塑料板(硬纸板)、环形玻璃搅拌棒.
(2)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式为(中和热数值为57.3kJ/mol)$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol.
(3)取55mLNaOH溶液和25mL硫酸溶液进行实验,实验数据如表.
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
(4)有关中和热测定实验,下列说法错误的是bc
a.用温度计测定NaOH溶液起始温度后马上直接测定H2SO4溶液的温度会导致中和热数值比57.3低
b.温度计的冲洗液应倒入小烧杯参与反应
c.混合硫酸和氢氧化钠溶液时应分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.若装置完全相同,操作均没失误,取110mLNaOH溶液和50mL硫酸溶液进行实验,误差比55mLNaOH溶液和25mL硫酸溶液进行实验误差小.
19.标准状况下,同体积的下列物质中所含有的分子数最多的是( )
| A. | CO2 | B. | H2 | C. | H2O | D. | O2 |
16.下列有关化合物的说法正确的是( )
| A. | 干冰的主要成分是H2O | B. | SO2可大量用于漂白食品 | ||
| C. | 吸入CO可导致人体中毒 | D. | 小苏打的主要成份是Na2CO3 |
17.化学与生产、生活密切相关.下列叙述正确的是( )
| A. | 我国古代四大发明之一黑火药由硫酸、硝酸和木炭按一定比例混合制成 | |
| B. | PH计不能用于酸碱中和滴定终点的判断 | |
| C. | 石油的分馏,煤的干馏、气化、液化均是物理变化 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
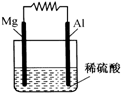 如图所示.
如图所示.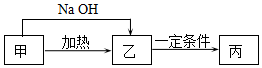 甲、乙、丙3种物质在生产生活中用途广泛,它们均是由短周期元素组成的化合物.甲含有4种元素,其中一种元素原子的最外层电子数是内层的2倍.
甲、乙、丙3种物质在生产生活中用途广泛,它们均是由短周期元素组成的化合物.甲含有4种元素,其中一种元素原子的最外层电子数是内层的2倍.