题目内容
6.某有机物的结构简式如图.下列关于该有机物叙述正确的是( )
| A. | 分子式为C9H11O5 | |
| B. | 可以分别与乙醇、乙酸在一定条件下反应,且反应类型相同 | |
| C. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且褪色原理相同 | |
| D. | 含有苯环的酯的同分异构体有4种 |
分析 有机物含有羧基,具有酸性,可发生中和、酯化反应,含有羟基,可发生取代、氧化反应,含有碳碳双键,可发生加成、加聚和氧化反应,以此解答该题.
解答 解:A.由结构简式可知分子式为C8H10O5,故A错误;
B.含有羧基、羟基,可发生酯化反应,故B正确;
C.含有碳碳双键,可与高锰酸钾发生氧化反应,与溴水发生加成反应,故C错误;
D.有机物含有3个双键,1个环,不饱和度为4,而含有苯环的酯的同分异构体不饱和度为5,故D错误.
故选B.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构特点和官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
16.标准状况下将VLHCl溶解在1L水中(水的密度近似为1g•mL-1),所得溶液的密度为ρg•mL-1,质量分数为w,物质浓度为c mol•L-1 ,则下列关系中不正确的是( )
| A. | ρ=$\frac{(36.5V+22400)c}{V}$ | B. | c=$\frac{1000Vρ}{36.5V+22400}$ | ||
| C. | V=$\frac{22400ω}{36.5(1-ω)}$ | D. | ρ=$\frac{36.5c}{1000ω}$ |
17.下列反应的离子方程式书写正确的是( )
| A. | 锌与CH3COOH溶液反应:Zn+2H+═Zn2++H2↑ | |
| B. | 氢氧化铝与稀硝酸反应:H++OH-═H2O | |
| C. | CuCl2溶液与铁粉反应:3Cu2++2Fe═3Cu+2Fe3+ | |
| D. | MgCl2溶液与氨水反应:Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+ |
11.有机物甲、乙的结构如图所示,下列说法正确的是( )
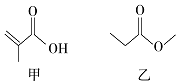
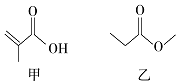
| A. | 甲、乙互为同分异构体 | |
| B. | 甲、乙都能发生取代、加成反应 | |
| C. | 与甲具有相同官能团的同分异构体还有2种 | |
| D. | 与乙具有相同官能团的同分异构体还有2种 |
18.短周期主族元素甲、乙、丙、丁、戊的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,甲和丙同主族,丁原子最外层电子数与电子层数相等,在中学常见的酸中戊的最髙价氧化物对应的水化物的酸性最强.下列叙述错误的是( )
| A. | 氧元素与甲、乙、丙形成的二元化合物均只有两种 | |
| B. | 简单离子半径:戊>乙>丙>丁 | |
| C. | 甲、乙、戊三种元素可形成含有共价键的离子化合物 | |
| D. | 丙、丁、戊三种元素的最高价氧化物对应的水化物两两之间均能发生反应 |
1.为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4+H2?CHCl3+HCl△H=QKJ•mol-1.已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.在密闭容器中,该反应达到平衡后,测得如下数据(不考虑副反应)
(1)110℃时平衡常数1
(2)实验1中,CCl4的转化率A为60%,平衡时c(CHCl3)=0.48mol/L
(3)实验2中,10小时后达到平衡,H2的平均反应速率为0.05mol/(L•h)
在此实验的平衡体系中,再加入1.0molCCl4和0.5molHCl,平衡将向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”);
(4)实验3中,B的值②
①等于50% ②大于50% ③小于50% ④无法判断
(5)能判断该反应已达到化学平衡状态的依据是BC
A.容器中压强不变
B.反应热△H不变
C.v正(H2)=v逆(HCl)
D.混合气体的密度保持不变.
| 实验序号 | 温度℃ | 初始CCl4浓度mol/L | 初始H2浓度mol/L | CCl4的平衡转化率 |
| 1 | 110 | 0.8 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 120 | 1 | 1 | B |
(2)实验1中,CCl4的转化率A为60%,平衡时c(CHCl3)=0.48mol/L
(3)实验2中,10小时后达到平衡,H2的平均反应速率为0.05mol/(L•h)
在此实验的平衡体系中,再加入1.0molCCl4和0.5molHCl,平衡将向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”);
(4)实验3中,B的值②
①等于50% ②大于50% ③小于50% ④无法判断
(5)能判断该反应已达到化学平衡状态的依据是BC
A.容器中压强不变
B.反应热△H不变
C.v正(H2)=v逆(HCl)
D.混合气体的密度保持不变.
2.下表各组物质中,物质之间不可能实现如图所示转化的是( )

| 选项 | X | Y | Z | M |
| A | Fe | FeCl2 | FeCl3 | Cl2 |
| B | Mg | C | CO | CO2 |
| C | NaOH | NaCO3 | NaHCO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A. | A | B. | B | C. | C | D. | D |