题目内容
15.下列关于铝及其化合物的叙述正确的是( )| A. | 铝罐可久盛食醋 | |
| B. | 铝与Fe2O3发生铝热反应,反应后固体物质增重 | |
| C. | 氢氧化铝可作胃酸的中和剂 | |
| D. | 明矾用作净水剂不涉及化学变化 |
分析 A、铝罐可与食醋反应;
B、铝与Fe2O3发生铝热反应,2mol铁转化为2mol的铝,反应后固体物质质量减小;
C、氢氧化铝是弱碱;
D、明矾在水中可以电离出两种金属离子K+、Al3+.而Al3+很容易水解,生成胶状的氢氧化铝,氢氧化铝胶体的吸附能力很强,可以吸附水里悬浮的杂质,从而使杂质沉降水变澄清.
解答 解:A、铝罐可与食醋反应,所以不能用铝罐可久盛食醋,故A错误;
B、铝与Fe2O3发生铝热反应,2mol铁转化为2mol的铝,反应后固体物质质量减小,而不是增加,故B错误;
C、氢氧化铝是弱碱,所以氢氧化铝可作胃酸的中和剂,故C正确;
D、明矾在水中可以电离出两种金属离子K+、Al3+.而Al3+很容易水解,生成胶状的氢氧化铝,氢氧化铝胶体的吸附能力很强,可以吸附水里悬浮的杂质,从而使杂质沉降水变澄清,属于化学变化,故D错误;
故选C.
点评 本题考查物理变化与化学变化的判断,难度不大.要注意化学变化和物理变化的本质区别是否有新物质生成.

练习册系列答案
相关题目
5.下列关于Fe及其化合物的性质的相关描述不正确的是( )
| A. | 生铁易被腐蚀,纯铁不易被腐蚀 | |
| B. | 常温下可用铁制容器来运输浓硫酸 | |
| C. | Fe2+的检验:取少量样品溶液,加入适量氯水,再滴2滴KSCN溶液,振荡观察 | |
| D. | 工业上常用稀盐酸或稀硫酸除铁锈 |
6.硅及其化合物在材料领域中应用广泛.下列说法正确的是( )
| A. | 光导纤维的主要成分是硅 | B. | 水晶项链的主要成分是硅酸盐 | ||
| C. | 晶体硅能用来制造太阳能电池 | D. | 二氧化硅是一种半导体材料 |
3.下列有关叙述正确的是( )
| A. | 蒸馏实验中温度计的水银球应插入溶液中 | |
| B. | SiO2既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物 | |
| C. | 分液时,先打开玻璃塞,再打开旋塞,使下层液体从下口流出,上层液体从上口倒出 | |
| D. | 开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应先关冷凝水再撤酒精灯 |
10.“绿色化学”是21世纪化学发展的主导方面.“绿色化学”要求从根本上消除污染,包括“绿色生产”和“绿色销毁”等内容.以下做法属于“绿色化学”的是( )
| A. | 将垃圾废物浇上汽油焚烧 | B. | 开发风能、太阳能等新能源 | ||
| C. | 让工业废水直接排入清江中 | D. | 杜绝污染源 |
20.830K时,在恒容密闭容器中进行的可逆反应:C(s)+H2O(g)?H2(g)+CO(g),下列哪种情况下,可说明该反应已经达到化学平衡状态( )
| A. | v正(C):v逆(H2)=1:1的状态 | |
| B. | 用H2O、CO、H2的物质的量浓度变化表示的反应速率的比为1:1:1的状态 | |
| C. | 混合气体的密度不再改变的状态 | |
| D. | 当平衡常数K不发生改变的时候 |
7.下列离子方程式正确的是( )
| A. | AlCl3溶液中加入氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 将氯气通入到水中:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+HCO3-═CaCO3↓+H2O | |
| D. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液 Fe2++2H++H2O2═Fe3++2H2O |
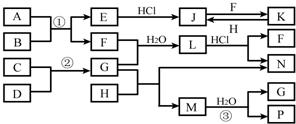 如图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去).
如图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去).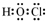 ;
;