题目内容
1.某硫酸盐RSO4在t℃时溶解度为31.7g,在t℃时取足量RSO4的饱和溶液,向其中加入8.00g无水RSO4后,析出24.6g RSO4•7H2O晶体,则R为( )| A. | Zn | B. | Cu | C. | Fe | D. | Mg |
分析 饱和溶液:在一定温度、一定量的溶剂中,溶质不能继续被溶解的溶液,依据此定义计算即可.
解答 解:由于析出溶质后,此溶液仍然为饱和溶液,设R的相对原子质量为M,依据题意有:$\frac{24.6×\frac{M+96}{M+96+7×18}}{24.6-8}×100%=\frac{31.7}{100+31.7}×%$,解得M=24,故此金属是Mg,故答案为:D.
点评 本题考查饱和溶液的计算问题,本题难度不大,做题时注意析出晶体后剩余溶液仍为饱和溶液,特别是形成结晶水合物这一点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列对生活中有关化学问题的分析不正确的是( )
| A. | 钙和磷都是人体内含量丰富的矿物元素,属于常量元素 | |
| B. | 白色污染是指聚乙烯、聚氯乙烯等各种废塑料制品造成的污染 | |
| C. | 具有强吸附性的活性炭能吸附某些溶于水中的杂质,并能对水进行消毒 | |
| D. | 青霉素等抗生素对某些微生物有抑制或杀灭作用,但对人体细胞的毒性很低 |
9.若短周期元素可以形成A2B3型化合物,则两种元素的原子序数之差不可能是( )
| A. | 1 | B. | 3 | C. | 5 | D. | 6 |
13.下列物质暴露在空气中,会发生风化的是( )
| A. | 食盐 | B. | 石碱 | C. | 烧碱 | D. | 氧化钙 |
10.下列过程中,属于化学变化的是( )
| A. | 石油分馏 | B. | 用蒸馏法制取蒸馏水 | ||
| C. | 干冰气化 | D. | 电解水制氧气 |
11.下列化学用语表示正确的是( )
| A. | Mg2+的结构示意图: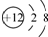 | |
| B. | 葡萄糖的结构简式:C6H12O6 | |
| C. | H2O2的电子式: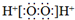 | |
| D. | 硫酸的电离方程式:H2SO4═H22++SO42- |
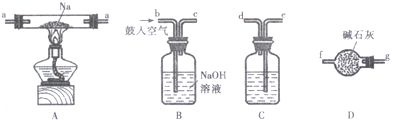
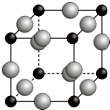 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):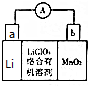 锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用,因此锂元素被誉为“能源元素”.请回答下列问题:
锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用,因此锂元素被誉为“能源元素”.请回答下列问题: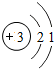 ;
;