题目内容
15.可逆反应:2NO2(g)?2NO(g)+O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是( )①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率数值之比为2:2:1的状态
④混合气体的颜色不再改变的状态.
| A. | ①④ | B. | ②③ | C. | ①③④ | D. | ①②③④ |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:①单位时间内生成n mol O2等效于消耗2n mol NO2,同时生成2n mol NO2,正逆反应速率相等,达平衡状态,故正确;
②单位时间内生成n mol O2的同时生成2n mol NO,都体现正反应方向,故错误;
③只要反应发生就符合NO2、NO、O2表示的反应速率数值之比为2:2:1的状态,故错误;
④混合气体的颜色不再改变的状态,说明二氧化氮的浓度不变,反应达平衡状态,故正确;
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
6.下列关于钠及其化合物的叙述中错误的是( )
| A. | 碳酸钠比碳酸氢钠的热稳定性要好 | |
| B. | 钠在空气中燃烧生成Na2O | |
| C. | 钠在发生化学反应时只作还原剂 | |
| D. | 钠单质暴露在空气中最终将变成Na2CO3 |
3.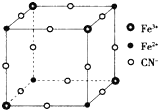 有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
 有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )| A. | 该晶体的化学式为MFe2(CN)6 | |
| B. | 该晶体熔融可导电,且属于化学变化 | |
| C. | 该晶体属于离子晶体,M呈+2价 | |
| D. | 晶体中与每个Fe3+距离最近且等距离的CN-为6个 |
10.下列叙述正确的是( )
| A. | 乙醇汽油是在汽油中加入适量乙醇而形成的一种燃料,它是一种新型化合物 | |
| B. | 用酸性KMnO4溶液不能鉴别CH3CH2CH2CH2OH和CH3CH2CH2COOH | |
| C. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 | |
| D. | 能说明苯不是单双键交替结构的事实是:苯的间二溴代物无同分异构体 |
20.我国科学家在世界上首次合成三种新核素,其中一种新核素的名称是铪-185,关于铪-185,下列说法中正确的是( )
①是一种新元素 ②是一种新原子 ③原子核内有185个质子 ④是铪-180的一种新的核素.
①是一种新元素 ②是一种新原子 ③原子核内有185个质子 ④是铪-180的一种新的核素.
| A. | ①和③ | B. | ②和④ | C. | ②和③ | D. | ③和④ |
7.下列除去杂质的方法正确的是( )
| A. | 除去乙烷中少量的乙烯:通过酸性KMnO4溶液进行分离 | |
| B. | 除去乙酸乙酯中少量的乙酸:用饱和氢氧化钠溶液洗涤、分液、干燥、蒸馏 | |
| C. | 除去CO2中少量的HCl气体:气体通过盛饱和碳酸钠溶液的洗气瓶 | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
4.下列关于物质分类的说法正确的是( )
①稀豆浆、硅酸、氯化铁溶液都属于胶体
②氯水、次氯酸都属于弱电解质
③Na2O、MgO、Al2O3均属于碱性氧化物
④明矾、冰水混合物、四氧化三铁都不是混合物
⑤电解熔融的Al2O3、12C 转化为14C 都属于化学变化
⑥葡萄糖、油脂都不属于有机高分子.
①稀豆浆、硅酸、氯化铁溶液都属于胶体
②氯水、次氯酸都属于弱电解质
③Na2O、MgO、Al2O3均属于碱性氧化物
④明矾、冰水混合物、四氧化三铁都不是混合物
⑤电解熔融的Al2O3、12C 转化为14C 都属于化学变化
⑥葡萄糖、油脂都不属于有机高分子.
| A. | ①② | B. | ②④ | C. | ③⑤ | D. | ④⑥ |
5.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面关于13C、15N叙述正确的是( )
| A. | 13C与15N有相同的中子数 | B. | 15N与14N互为同位素 | ||
| C. | 13C与C60互为同素异形体 | D. | 15N的核外电子数与中子数相同 |