题目内容
某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链.其主要工艺如下:

(1)写出工业上电解食盐水反应的化学方程式 .
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式: .
(3)已知:①Mg(s)+Cl2(g)═MgCl2(s);△H=-641kJ?mol-1
②Ti(s)+2Cl2(g)═TiCl4(s);△H═-770kJ?mol-1
则2Mg(s)+TiCl4(g)═2MgCl2(s)+Ti(s);△H═ ,反应2Mg+TiCl4
2MgCl4+Ti在Ar气氛中进行的理由是 .
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池中正极上的电极反应式是 ,负极区的pH (填“增大”、“减小”、“不变”).

(1)写出工业上电解食盐水反应的化学方程式
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式:
(3)已知:①Mg(s)+Cl2(g)═MgCl2(s);△H=-641kJ?mol-1
②Ti(s)+2Cl2(g)═TiCl4(s);△H═-770kJ?mol-1
则2Mg(s)+TiCl4(g)═2MgCl2(s)+Ti(s);△H═
| ||
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池中正极上的电极反应式是
考点:热化学方程式,原电池和电解池的工作原理,电解原理
专题:化学反应中的能量变化
分析:(1)电解食盐水生成NaOH、H2和Cl2,以此书写离子方程式;
(2)钛铁矿经氯化得到四氯化钛、氯化铁和一氧化碳;依据原子守恒配平写出;
(3)根据盖斯定律,①×2-②可得;Mg和Ti都有较强还原性,在高温下都易被空气中的O2氧化;
(4)碱性甲醇电池中,O2在正极得电子发生还原反应,负极甲醇消耗氢氧根离子生成碳酸盐;
(2)钛铁矿经氯化得到四氯化钛、氯化铁和一氧化碳;依据原子守恒配平写出;
(3)根据盖斯定律,①×2-②可得;Mg和Ti都有较强还原性,在高温下都易被空气中的O2氧化;
(4)碱性甲醇电池中,O2在正极得电子发生还原反应,负极甲醇消耗氢氧根离子生成碳酸盐;
解答:
解:(1)电解食盐水生成NaOH、H2和Cl2,反应的化学方程式为:2NaCl+2H2 O
2NaOH+H2↑+Cl2↑;
故答案为:2NaCl+2H2 O
2NaOH+H2↑+Cl2↑;
(2)从图示可知氯化时的反应物为FeTiO3、C、Cl2,生成物为FeCl3、TiCl4、CO,再根据得失电子和原子守恒即可得出该反应的方程式为2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO,
故答案为:2FeTiO3+6C+7Cl2 =2FeCl3+2TiCl4+6CO;
(3)反应2Mg(s)+TiCl4(l)═2MgCl2(s)+Ti(s)可看做反应①×2-②得到,根据盖斯定律得△H-641kJ/mol×2-(-770 kJ/mol)=-512kJ?mol-1,反应2Mg(s)+TiCl4(l)═2MgCl2(s)+Ti(s)在Ar气氛中进行的理由是Mg和Ti都有较强还原性,在高温下都易被空气中的O2氧化;
故答案为:-512 kJ?mol-1;Mg和Ti都有强还原性,在Ar气氛中可以防止被氧化;
(4)碱性甲醇电池中,O2在正极得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,负极电极反应为:CH3OH-6e-+OH-=CO32-+H2O,负极附近消耗氢氧根离子,溶液PH减小;
故答案为:O2+2H2O+4e-=4OH-,减小;
| ||
故答案为:2NaCl+2H2 O
| ||
(2)从图示可知氯化时的反应物为FeTiO3、C、Cl2,生成物为FeCl3、TiCl4、CO,再根据得失电子和原子守恒即可得出该反应的方程式为2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO,
故答案为:2FeTiO3+6C+7Cl2 =2FeCl3+2TiCl4+6CO;
(3)反应2Mg(s)+TiCl4(l)═2MgCl2(s)+Ti(s)可看做反应①×2-②得到,根据盖斯定律得△H-641kJ/mol×2-(-770 kJ/mol)=-512kJ?mol-1,反应2Mg(s)+TiCl4(l)═2MgCl2(s)+Ti(s)在Ar气氛中进行的理由是Mg和Ti都有较强还原性,在高温下都易被空气中的O2氧化;
故答案为:-512 kJ?mol-1;Mg和Ti都有强还原性,在Ar气氛中可以防止被氧化;
(4)碱性甲醇电池中,O2在正极得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,负极电极反应为:CH3OH-6e-+OH-=CO32-+H2O,负极附近消耗氢氧根离子,溶液PH减小;
故答案为:O2+2H2O+4e-=4OH-,减小;
点评:本题考查化学方程式的书写及计算、盖斯定律等,题目难度中等,注意根据盖斯定律解题.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题: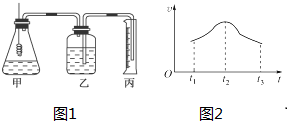
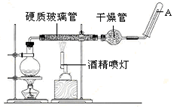 常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.