题目内容
 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:(1)P和Cl2反应生成PCl5的热化学方程式是
(2)PCl3和Cl2化合成PCl5的反应是可逆的.温度T1时在密闭容器中加入0.80molPCl5,反应达到平衡时PCl5还剩0.60mol,则PCl5的分解率α1等于
若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,则α2
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温再使PCl3和Cl2反应生成PCl5.原因是
考点:热化学方程式,化学平衡的计算
专题:化学反应中的能量变化,化学平衡专题
分析:(1)根据图象及反应热知识分析标注物质聚集状态对应反应焓变写出;
(2)根据热化学反应方程式的书写原则及化学平衡知识分析;
(3)根据化学平衡移动原理分析;
(2)根据热化学反应方程式的书写原则及化学平衡知识分析;
(3)根据化学平衡移动原理分析;
解答:
解:(1)热化学方程式书写要求:注明各物质的聚集状态,判断放热反应还是吸热反应,反应物的物质的量与反应热成对应的比例关系,根据图示P(s)+Cl2(g)→PCl5(g),反应物的总能量大于生成物的总能量,该反应是放热反应,反应热为△H=-306 kJ/mol+(-93KJ/mol)=-399KJ/mol,热化学方程式为:P(s)+
Cl2(g)═PCl5(g);△H=-399kJ/mol,
故答案为:P(s)+
Cl2(g)═PCl5(g);△H=-399kJ?mol-1;
(2)△H=生成物总能量-反应物总能量,Cl2(g)+PCl3(g)=PCl5(g),中间产物的总能量大于最终产物的总能量,该反应是放热反应,所以 PCl5(g)=PCl3(g)+Cl2(g)是吸热反应;热化学方程式:PCl5(g)=PCl3(g)+Cl2(g);△H=+93 kJ/mol,
PCl5分解率α1=
×100%=25%.PCl5(g)=PCl3(g)+Cl2(g)是吸热反应;升高温度向吸热反应方向移动,正反应(分解反应是吸热反应)是吸热反应,升高温度向正反应方向移动,转化率增大,α2 >α1 ;
故答案为:25%;大于;
(3)Cl2(g)+PCl3(g)=PCl5(g),是放热反应,降温平衡向放热反应方向移动,降温有利于PCl5(g)的生成,
故答案为:两步反应均为放热反应,降低温度有利于提高产率,防止产物分解;
| 5 |
| 2 |
故答案为:P(s)+
| 5 |
| 2 |
(2)△H=生成物总能量-反应物总能量,Cl2(g)+PCl3(g)=PCl5(g),中间产物的总能量大于最终产物的总能量,该反应是放热反应,所以 PCl5(g)=PCl3(g)+Cl2(g)是吸热反应;热化学方程式:PCl5(g)=PCl3(g)+Cl2(g);△H=+93 kJ/mol,
PCl5分解率α1=
| 0.8mol-0.6mol |
| 0.8mol |
故答案为:25%;大于;
(3)Cl2(g)+PCl3(g)=PCl5(g),是放热反应,降温平衡向放热反应方向移动,降温有利于PCl5(g)的生成,
故答案为:两步反应均为放热反应,降低温度有利于提高产率,防止产物分解;
点评:本题考查热化学方程式的书写、化学平衡计算、外界条件对化学平衡移动的影响及反应热的计算等知识.解题中需注意:热化学方程式中没有标注各物质的聚集状态,各物质的物质的量与反应热没有呈现对应的比例关系,不能正确判断放热反应和吸热反应,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列电解质在水溶液中电离方程式正确的是( )
| A、Ca(OH)2═Ca2++OH- | |||||||
| B、KClO3═K++Cl-+3O2- | |||||||
C、Na2CO3═Na2++CO
| |||||||
| D、HCl═H++Cl- |
下列关于酸、碱、盐元素组成的说法中,正确的是( )
| A、酸、碱一定含氢,盐一定不含氢 |
| B、酸、碱、盐可能都不含金属元素 |
| C、碱、盐可能含氧,酸一定含氧 |
| D、盐一定含金属元素,酸、碱不一定含金属元素 |
下列关于氧化还原反应的说法不正确的是( )
| A、反应SiO2+3C═SiC+2CO中,氧化剂与还原剂的物质的量之比为1:2 |
| B、向蔗糖中加入浓硫酸,蔗糖变黑,并有刺激性气味,说明浓硫酸具有脱水性和强氧化性 |
| C、浓硫酸、浓硝酸在加热条件下都能将木炭氧化为二氧化碳 |
| D、铁粉与足量稀硝酸反应时,氧化剂与还原剂的物质的量之比为2:3 |
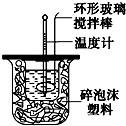 如图装置测定中和热的实验步骤如下:
如图装置测定中和热的实验步骤如下: 图中每一方格表示有关的一种反应物或生成物.已知B是一种单质,其余物质都是含有B元素的化合物;C是一种钠盐;E是C对应的酸;B和D的晶体都是高熔点、坚硬的固体,且D为B的氧化物(其他不含B元素的反应物以及各步反应添加的必要试剂和反应条件均被略去).
图中每一方格表示有关的一种反应物或生成物.已知B是一种单质,其余物质都是含有B元素的化合物;C是一种钠盐;E是C对应的酸;B和D的晶体都是高熔点、坚硬的固体,且D为B的氧化物(其他不含B元素的反应物以及各步反应添加的必要试剂和反应条件均被略去).