题目内容
9.某同学查阅资料后设计了一条1-丁醇的合成路线: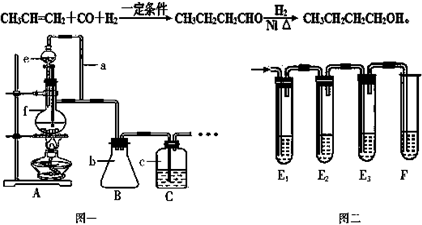
(1)利用图一装置可制备CO、丙烯等原料气体.①装置中e的名称是分液漏斗;②a的作用平衡内外压强,保证液体顺畅流下;
(2)实验室常用浓硫酸与甲酸作用来制备CO.写出对应的化学方程式:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O.
(3)制CO时,伴随的副产物还有少量SO2、CO2气体,某同学设计用图二装置进行检验.
①E1的作用是:检验产物是否有S02;E3的作用是:检验S02是否除尽;
②判断产物中有CO2的现象是E3中品红不褪色,F中石灰水变浑浊
(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是D;
A.高温、常压、催化剂 B.适当的温度、常压、催化剂
C.低温、高压、催化剂 D.适当的温度、高压、催化剂
(5)正丁醛经催化加氢得到含少量正丁醛的1一丁醇粗品,为提纯1-丁醇,该小组查阅文献得知:①R-CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓;②沸点:乙醚34℃,1-丁醇118℃.并设计出如下提纯路线:

试剂1为饱和NaHSO3溶液,操作2为萃取,操作3为蒸馏.
分析 CO的制备方法:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O,在题给装置中,导管a平衡分液漏斗内压强,使分液漏斗内的液体浓硫酸顺利滴下,b主要是起安全瓶的作用,以防止倒吸;c为除去CO中的酸性气体,选用NaOH溶液,还需用浓硫酸除去CO中的H2O,
(1)①根据装置图中e的构造可知e为分液漏斗;
②为了使产生的气体能顺利的从发生装置中排出,就必需保持压强一致,因此a的作用是保持恒压;
(2)甲酸在浓硫酸作用下脱水生成CO,根据元素守恒和元素守恒可书写化学方程式;
(3)要检验CO中少量S02、C02气体,用品红检验二氧化硫,并用酸性高锰酸钾除去二氧化硫,再用品红检验是否除尽,用石灰水检验二氧化碳,所以E1中装置品红溶液,E2中装置酸性高锰酸钾溶液,E3中装品红溶液,F中装澄清石灰水;
(4)题给合成正丁醛的反应为气体体积减小的放热反应,为增大反应速率和提高原料气的转化率;
(5)根据题中物质提纯的流程,粗品中含有正丁醛,利用信息①可知饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;加入乙醚的目的是萃取溶液中的1-丁醇,1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开.
解答 解:CO的制备方法:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O,在题给装置中,导管a平衡分液漏斗内压强,使分液漏斗内的液体浓硫酸顺利滴下,b主要是起安全瓶的作用,以防止倒吸;c为除去CO中的酸性气体,选用NaOH溶液,还需用浓硫酸除去CO中的H2O,
(1)①根据仪器e的构造可知e为分液漏斗,
故答案为:分液漏斗;
②CO的制备方法为:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O,反应中有气体产生,为了平衡分液漏斗内压强,使分液漏斗内的液体浓硫酸顺利滴下,所以使用了导管a,
故答案为:平衡内外压强,保证液体顺畅流下;
(2)甲酸在浓硫酸作用下脱水生成CO气体和水,反应的化学方程式为:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O,
故答案为:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O;
(3)要检验CO中少量S02、C02气体,用品红检验二氧化硫,并用酸性高锰酸钾除去二氧化硫,再用品红检验是否除尽,用石灰水检验二氧化碳,所以E1中装置品红溶液,E2中装置酸性高锰酸钾溶液,E3中装品红溶液,F中装澄清石灰水,
①根据上面的分析可知,E1的作用是:检验产物是否有S02,E3的作用是检验S02是否除尽,
故答案为:检验产物是否有S02;检验S02是否除尽;
②判断产物中有CO2的现象是E3中品红不褪色,F中石灰水变浑浊,
故答案为:E3中品红不褪色,F中石灰水变浑浊;
(4)由于反应是一个体积减小的可逆反应,所以采用高压,有利于增大反应速率和提高原料气的转化率;正向反应是放热反应,虽然低温有利于提高原料气的转化率,但不利于增大反应速率,因此要采用适当的温度;催化剂不能提高原料气的转化率,但有利于增大反应速率,缩短到达平衡所需要的时间,故正确所选项是D,
故答案为:D;
(5)粗品中含有正丁醛,根据所给的信息利用饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;由于饱和NaHSO3溶液是过量的,所以加入乙醚的目的是萃取溶液中的1-丁醇;因为1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开,
故答案为:饱和NaHSO3溶液;萃取;蒸馏.
点评 本题考查制备方案的设计,题目难度中等,涉及气体的制备、有机物的分离、提纯方法、醇的性质以及对基础知识和基本操作的考查,答题时注意把握基础知识和基本实验操作的灵活运用,试题培养了学生的分析、理解能力及化学实验能力.

 阅读快车系列答案
阅读快车系列答案| A. | Na Mg Al | B. | Na O F | C. | P Si Al | D. | C Si P |
| A. | 随着核电荷数增加,碱金属单质的密度逐渐增大 | |
| B. | 随着核电荷数增加,卤素单质的熔沸点逐渐降低 | |
| C. | 随着核电荷数的增加,碱金属单质与水反应的剧烈程度增大 | |
| D. | 随着核电荷数增加,碱金属离子的氧化性逐渐增强,卤素离子的还原性逐渐减弱 |
| A. | 质子数为235 | B. | 中子数为92 | C. | 电子数为143 | D. | 质量数为235 |
| A. | 元素非金属性由弱到强的顺序为Z<Y<X | |
| B. | Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 | |
| C. | 3种元素的气态氢化物中,Z的气态氢化物最稳定 | |
| D. | 原子半径由大到小的顺序为Z>Y>X |
| A. | 碳碳双键不可旋转所以烯烃一定有顺反异构 | |
| B. | 邻二甲苯只有一种结构可以证明苯分子中无单双健的交替结构 | |
| C. | CH2Cl2无同分异构体可以证明CH4是正四面体的结构 | |
| D. | 乙烯、乙炔是平面型分子,可知CH3-CH=C(CH3)-C≡C-CH3分子中所有的碳原子共面 |


 、
、 ;
;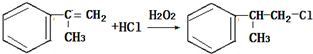

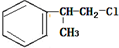
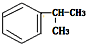 的一种同分异构体D符合以下条件:①苯环上有两条侧链 ②苯环上的一氯代物有2种,则D的结构简式为
的一种同分异构体D符合以下条件:①苯环上有两条侧链 ②苯环上的一氯代物有2种,则D的结构简式为 .
.