题目内容
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
H2(g)+
O2(g)=H2O(g)△H2
C(s)+O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
H2(g)+
| 1 |
| 2 |
C(s)+O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
| A、12△H3+10△H2-2△H1 |
| B、2△H1-10△H2-12△H3 |
| C、12△H3-10△H2-2△H1 |
| D、△H1-10△H2-12△H3 |
考点:有关反应热的计算
专题:
分析:根据盖斯定律,利用已知方程式的加减得出目标方程式C3H5(ONO2)3分解成CO2、N2、H2O、O2的化学方程式,其反应热也要相应的加减.
解答:
解:已知:①6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
②H2(g)+
O2(g)=H2O(g)△H2
③C(s)+O2(g)═CO2(g)△H3
由盖斯定律:10×②+12×③-2×①得:4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)△H=12△H3+10△H2-2△H1;
故选A.
②H2(g)+
| 1 |
| 2 |
③C(s)+O2(g)═CO2(g)△H3
由盖斯定律:10×②+12×③-2×①得:4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)△H=12△H3+10△H2-2△H1;
故选A.
点评:本题考查了反应热的计算,侧重于盖斯定律应用的考查,题目难度不大,构建目标方程式是解答关键.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
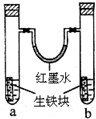 如图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入一块生铁,放置一段时间.下列有关描述错误的是( )
如图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入一块生铁,放置一段时间.下列有关描述错误的是( )| A、两边生铁块中的碳均为各自形成的原电池的正极 |
| B、a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 |
| C、两试管中相同的电极反应式是:Fe-2e-=Fe2+ |
| D、红墨水柱两边的液面变为左低右高 |
下列溶液中NO3-的物质的量最大的是( )
| A、500 mL 1 mol/L的KNO3溶液 |
| B、500 mL 1 mol/L的Ba(NO3)2溶液 |
| C、100 mL 0.5 mol/L的Mg(NO3)2溶液 |
| D、1 L 0.5 mol/L的Fe(NO3)3溶液 |
下列化学用语的表达正确的是( )
A、Na2SO4电离:Na2SO4=Na2++SO
| ||
B、Cl-的结构示意图: | ||
C、质子数为6,中子数为8的微粒:
| ||
| D、医用“钡餐”的化学式:BaSO4 |