题目内容
 近几年地球发生地震灾害较多,抢救地震后被困在废墟下的伤员,首要的措施是给伤员补充能量.如图是医院给伤员输液时用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列的内容后填写:
近几年地球发生地震灾害较多,抢救地震后被困在废墟下的伤员,首要的措施是给伤员补充能量.如图是医院给伤员输液时用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列的内容后填写:(1)葡萄糖的摩尔质量为
(2)该溶液中含水
(3)该溶液的密度约为
(4)该溶液的物质的量浓度为
考点:物质的量浓度的相关计算
专题:计算题
分析:(1)葡萄糖的摩尔质量在数值上等于它的相对分子质量,单位是g/mol;
(2)根据标签给出的数据可知,250ml葡萄糖注射液中含葡萄糖12.5g,含量为5%,根据“葡萄糖质量÷葡萄糖含量”计算出一瓶葡萄糖注射液的质量;根据溶液中含水的质量=葡萄糖注射液的质量×水的含量(1-葡萄糖质量分数);
(3)根据溶液的密度=一瓶葡萄糖注射液的质量÷体积来计算;
(4)先根据葡萄糖的质量求出它的物质的量,然后代入公式C=
求出溶液的物质的量浓度.
(2)根据标签给出的数据可知,250ml葡萄糖注射液中含葡萄糖12.5g,含量为5%,根据“葡萄糖质量÷葡萄糖含量”计算出一瓶葡萄糖注射液的质量;根据溶液中含水的质量=葡萄糖注射液的质量×水的含量(1-葡萄糖质量分数);
(3)根据溶液的密度=一瓶葡萄糖注射液的质量÷体积来计算;
(4)先根据葡萄糖的质量求出它的物质的量,然后代入公式C=
| n |
| V |
解答:
解:(1)葡萄糖的相对分子质量为:12×6+12+16×6=180,所以葡萄糖的摩尔质量为:180g/mol,故答案为:180g/mol;
(2)由于溶液中溶质的质量分数为5%,且含有共12.5g葡萄糖,一瓶葡萄糖注射液溶液的质量=12.5g÷5%=250g,所以该溶液中含水的质量=250g×(1-5%)=237.5g;故答案为:237.5.
(3)溶液的密度=
=
=1g/mL,即1g/cm3,故答案为:1;
(4)葡萄糖物质的量为n(C6H12O6)=
,所以溶液的物质的量浓度C(C6H12O6)=
=0.28mol?L-1,故答案为:0.28.
(2)由于溶液中溶质的质量分数为5%,且含有共12.5g葡萄糖,一瓶葡萄糖注射液溶液的质量=12.5g÷5%=250g,所以该溶液中含水的质量=250g×(1-5%)=237.5g;故答案为:237.5.
(3)溶液的密度=
| m |
| V |
| 250g |
| 250mL |
(4)葡萄糖物质的量为n(C6H12O6)=
| 12.5g |
| 180g/mol |
| 12.5g | ||
|
点评:本题考查了物质的量浓度的有关计算,熟记公式的使用以及物质的结构是解题关键,难度不大.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
已知氧化还原反应可以看成是有化合价升降的反应,氧化剂得电子化合价降低,还原剂失电子化合价升高,还原剂把电子转移给氧化剂.在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+,MnO4-→Mn2+,Cl2→Cl-,HNO2→NO.如果分别用等量的这些物质氧化足量的KI,得到I2最多的是( )
| A、Fe3+ |
| B、MnO4- |
| C、Cl2 |
| D、HNO2 |
下列化学用语正确的是( )
| A、乙烯的分子式:CH2═CH2 |
| B、次氯酸分子的结构式:H-O-Cl |
C、羟基的电子式: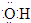 |
| D、以铁作阳极电解时,阳极的电极反应式:Fe-3e-═Fe3+ |
 单质硼有无定形和晶体两种,参考下列数据.
单质硼有无定形和晶体两种,参考下列数据.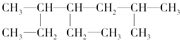
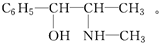
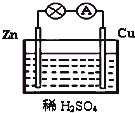 如图为原电池的示意图.请回答:
如图为原电池的示意图.请回答: