题目内容
下列化学用语正确的是( )
| A、乙烯的分子式:CH2═CH2 |
| B、次氯酸分子的结构式:H-O-Cl |
C、羟基的电子式: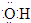 |
| D、以铁作阳极电解时,阳极的电极反应式:Fe-3e-═Fe3+ |
考点:分子式,电子式,结构式,电极反应和电池反应方程式
专题:化学用语专题
分析:A、乙烯的分子式为C2H4;
B、次氯酸分子以氧原子为中心原子,其结构式为H-O-Cl;
C、羟基是缺电子基团,其电子式为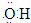 ;
;
D、以铁作阳极电解时,铁失去电子生成二价铁离子.
B、次氯酸分子以氧原子为中心原子,其结构式为H-O-Cl;
C、羟基是缺电子基团,其电子式为
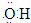 ;
;D、以铁作阳极电解时,铁失去电子生成二价铁离子.
解答:
解:A、乙烯的分子式为C2H4,CH2═CH2为乙烯的结构简式;
B、次氯酸分子以氧原子为中心原子,其结构式为H-O-Cl;
C、羟基是缺电子基团,其电子式为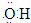 ;
;
D、以铁作阳极电解时,铁失去电子生成二价铁离子,阳极的电极反应式:Fe-2e-═Fe2+.
故选:B.
B、次氯酸分子以氧原子为中心原子,其结构式为H-O-Cl;
C、羟基是缺电子基团,其电子式为
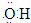 ;
;D、以铁作阳极电解时,铁失去电子生成二价铁离子,阳极的电极反应式:Fe-2e-═Fe2+.
故选:B.
点评:本题考查了常见化学用语的表示,题目难度不大,注意掌握常见化学用语的正确表示方法.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
在一个定容密闭容器中,加入2molA和1molB发生如下反应:2A(g)+B(g)?3C(g)+D(g),达到平衡时C的浓度为1.2mol/L.若维持温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2mol/L的是( )
| A、4 mol A+2 mol B |
| B、1.5mol C+0.5 mol D+0.5mol B+1 molA |
| C、3 mol C+1 mol D |
| D、1.6 mol A+0.8 mol B+0.6 mol C+0.3 mol D |
2009年卫生部印发了《饮水型地方性砷中毒监测方案(试行)的通知》.已知在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+═2As+3SnCl62-+6M,关于该反应的说法中正确的组合是( )
①SnCl2是还原剂
②还原性:Cl->As
③每生成7.5gAs,还原剂失去的电子为0.3mol
④M为H2O
⑤SnCl62-是氧化产物.
①SnCl2是还原剂
②还原性:Cl->As
③每生成7.5gAs,还原剂失去的电子为0.3mol
④M为H2O
⑤SnCl62-是氧化产物.
| A、①③④⑤ | B、①②④⑤ |
| C、①②③④ | D、①③ |
下列各组离子能在指定环境中大量共存的是( )
A、c(HCO
| ||||||
B、室温下,由水电离出的c(H+)=1×10-12 mol?L-1的溶液中:Fe2+、ClO-、Na+、SO
| ||||||
C、无色透明溶液中:SO
| ||||||
D、使红色石蕊试纸变蓝的溶液中:SO
|
下列各物质溶液中,指定微粒浓度之间的关系不正确的是( )
| A、饱和NH4Cl溶液中:c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
| B、0.1mol/LNaHCO3溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol/L |
| C、饱和NaHS溶液中:c(Na+)>c(HS-)>c(H+)>c(OH-) |
| D、0.1mol/LCH3COONa溶液中:c(CH3COO-)>c(OH-) |
在一定条件下,测得2CO2?2CO+O2(反应从CO2开始)平衡体系的平均相对分子质量为M,在此条件下,CO2的分解率为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
 近几年地球发生地震灾害较多,抢救地震后被困在废墟下的伤员,首要的措施是给伤员补充能量.如图是医院给伤员输液时用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列的内容后填写:
近几年地球发生地震灾害较多,抢救地震后被困在废墟下的伤员,首要的措施是给伤员补充能量.如图是医院给伤员输液时用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列的内容后填写: