题目内容
有一无色透明的稀溶液能与铝作用放出氢气,试分析下列离子中:H+、Ba2+、Mg2+、OH-、SO32-、Cl-、CO32-、NO3-,可能有哪些离子大量存在于此溶液中.
第一种情况:有 ,可能有 .
第二种情况:有 ,可能有 .
第一种情况:有
第二种情况:有
考点:离子共存问题
专题:
分析:溶液无色,则一定不存在有色的离子,与铝反应生成氢气,则溶液中存在大量氢离子或氢氧根离子,
(1)当生成Al3+时,说明溶液呈酸性,因在含HNO3的溶液中放入Al不生成H2,则一定不存在NO3-离子,与H+离子反应的离子不能大量共存;
(2)当生成AlO2-时,说明溶液呈碱性,溶液中存在大量的OH-离子,与OH-离子反应的离子不能大量共存,以此解答该题.
(1)当生成Al3+时,说明溶液呈酸性,因在含HNO3的溶液中放入Al不生成H2,则一定不存在NO3-离子,与H+离子反应的离子不能大量共存;
(2)当生成AlO2-时,说明溶液呈碱性,溶液中存在大量的OH-离子,与OH-离子反应的离子不能大量共存,以此解答该题.
解答:
解:溶液无色,则一定不存在有色离子,与铝反应生成氢气,则溶液中存在大量H+或OH-,
(1)当生成Al3+时,说明溶液呈酸性,因在含HNO3的溶液中放入Al不生成H2,则一定不存在NO3-离子;酸性溶液中不存在SO32-、CO32-、OH-离子,根据溶液电荷守恒,则溶液中一定存在阴离子,即Cl-离子一定存在,即有H+、Cl-,则可能大量存在的离子为Ba2+、Mg2+,
故答案为:H+、Cl-;Ba2+、Mg2+;
(2)当生成AlO2-时,说明溶液呈碱性,溶液中存在大量的OH-离子,与OH-反应的Mg2+、H+离子不能大量存在;根据溶液电荷守恒,则溶液中一定存在阳离子,即Ba2+离子一定存在,而Ba2+与SO32-离子生成难溶于水的沉淀,则一定不存在SO32-离子,则可能大量存在Cl-、NO3-,
故答案为:OH-、Ba2+;Cl-、NO3-.
(1)当生成Al3+时,说明溶液呈酸性,因在含HNO3的溶液中放入Al不生成H2,则一定不存在NO3-离子;酸性溶液中不存在SO32-、CO32-、OH-离子,根据溶液电荷守恒,则溶液中一定存在阴离子,即Cl-离子一定存在,即有H+、Cl-,则可能大量存在的离子为Ba2+、Mg2+,
故答案为:H+、Cl-;Ba2+、Mg2+;
(2)当生成AlO2-时,说明溶液呈碱性,溶液中存在大量的OH-离子,与OH-反应的Mg2+、H+离子不能大量存在;根据溶液电荷守恒,则溶液中一定存在阳离子,即Ba2+离子一定存在,而Ba2+与SO32-离子生成难溶于水的沉淀,则一定不存在SO32-离子,则可能大量存在Cl-、NO3-,
故答案为:OH-、Ba2+;Cl-、NO3-.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、NaHSO4 溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| B、向FeCl2溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| C、向Ca(ClO)2溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3- |
| D、FeSO4酸性溶液中加H2O2:2Fe2++H2O2=2Fe3++2OH- |
 某温度下,相同pH值的盐酸和醋酸溶液,pH值随溶液体积变化的曲线如图,据图判断正确的是( )
某温度下,相同pH值的盐酸和醋酸溶液,pH值随溶液体积变化的曲线如图,据图判断正确的是( )| A、Ⅱ为盐酸稀释时pH值变化曲线 |
| B、a点Kw的数值比c点Kw的数值大 |
| C、b点溶液的导电性比c点溶液的导电性强 |
| D、b点酸的总浓度大于a点酸的总浓度 |
 将0.1mol A12O3、0.1mol SiO2和一定量的Fe2O3、NaOH的固体混合物溶于水,充分反应后,向所得反应体系中缓缓通人0.5mol HC1气体,所得难溶物的物质的量与HC1的物质的量的关系如图所示.下列说法正确的是( )
将0.1mol A12O3、0.1mol SiO2和一定量的Fe2O3、NaOH的固体混合物溶于水,充分反应后,向所得反应体系中缓缓通人0.5mol HC1气体,所得难溶物的物质的量与HC1的物质的量的关系如图所示.下列说法正确的是( )| A、Fe2O3、NaOH的物质的量分别是0.1mol、0.5mol |
| B、结合H+的能力:SiO32->AlO2- |
| C、A点溶液呈碱性,B、C两点溶液呈中性 |
| D、当n(HCl)>0.5mol时,难溶物的量会继续增多 |
一定温度下,将2molX和1molY通入体积为1L的密闭容器中,发生反应2X(g)+Y(g)?2Z(g)△H<0,其中Z的浓度随时间变化的数据如下表所示:
下列说法不正确的是( )
| 时间 | 0min | 2min | 4min | 6min | 8min | 10min |
| Z的浓度mol/L | 0 | 0.8 | 1.2 | 1.4 | 1.4 | 1.4 |
| A、用Y来表示0-4min的平均反应速率为0.15mol/(L?min) |
| B、该温度下反应的化学平衡常数为18.15 |
| C、向平衡体系中再加入2molX和1mol Y,达到新的平衡时X的体积分数增大 |
| D、对平衡体系降低温度,化学反应后速率减慢,但Y的转化率增大 |
X和Y都是短周期元素,有aXn-和bYm+两种简单离子,已知aXn-比bYm+多两个电子层,则下面关系式或说法中正确的是( )
| A、X只能是第三周期元素 |
| B、a-b+n+m=10或16 |
| C、b不大于6 |
| D、Y不可能是第二周期元素 |
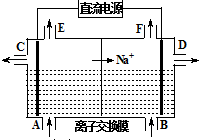 电解原理在工业生产中有广泛的应用.
电解原理在工业生产中有广泛的应用. 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.