题目内容
一定温度下,将2molX和1molY通入体积为1L的密闭容器中,发生反应2X(g)+Y(g)?2Z(g)△H<0,其中Z的浓度随时间变化的数据如下表所示:
下列说法不正确的是( )
| 时间 | 0min | 2min | 4min | 6min | 8min | 10min |
| Z的浓度mol/L | 0 | 0.8 | 1.2 | 1.4 | 1.4 | 1.4 |
| A、用Y来表示0-4min的平均反应速率为0.15mol/(L?min) |
| B、该温度下反应的化学平衡常数为18.15 |
| C、向平衡体系中再加入2molX和1mol Y,达到新的平衡时X的体积分数增大 |
| D、对平衡体系降低温度,化学反应后速率减慢,但Y的转化率增大 |
考点:化学平衡的计算
专题:化学平衡专题
分析:A、反应速率V=
计算反应速率,速率之比等于化学方程式计量数之比计算分析;
B、结合化学平衡三段式列式计算平衡浓度,依据平衡常数概念计算得到平衡常数判断;
C、向平衡体系中再加入2molX和1mol Y,相当于增大压强,反应是气体减小的反应,平衡正向进行;
D、反应是放热反应,降低温度,反应速率减小,平衡正向进行.
| △c |
| △t |
B、结合化学平衡三段式列式计算平衡浓度,依据平衡常数概念计算得到平衡常数判断;
C、向平衡体系中再加入2molX和1mol Y,相当于增大压强,反应是气体减小的反应,平衡正向进行;
D、反应是放热反应,降低温度,反应速率减小,平衡正向进行.
解答:
解:A、反应速率V=
计算反应速率,0-4min的Z平均反应速率=
=0.3mol/L?min,速率之比等于化学方程式计量数之比,V(Y)=
V(Z)=
×0.3mol/L?min=0.15mol/L?min,故A正确;
B、结合化学平衡三段式列式计算平衡浓度,
2X(g)+Y(g)?2Z(g)
起始浓度 2 1 0
变化浓度 1.4 0.7 1.4
平衡浓度 0.6 0.3 1.4
依据平衡常数概念计算得到平衡常数K=
=18.15,故B正确;
C、向平衡体系中再加入2molX和1mol Y,相当于增大压强,反应是气体减小的反应,平衡正向进行,达到新的平衡时X的体积分数减小,故C错误;
D、反应是放热反应,降低温度,反应速率减小,平衡正向进行,Y的转化率增大,故D正确;
故选C.
| △c |
| △t |
| 1.2mol/L |
| 4min |
| 1 |
| 2 |
| 1 |
| 2 |
B、结合化学平衡三段式列式计算平衡浓度,
2X(g)+Y(g)?2Z(g)
起始浓度 2 1 0
变化浓度 1.4 0.7 1.4
平衡浓度 0.6 0.3 1.4
依据平衡常数概念计算得到平衡常数K=
| 1.42 |
| 0.62×0.3 |
C、向平衡体系中再加入2molX和1mol Y,相当于增大压强,反应是气体减小的反应,平衡正向进行,达到新的平衡时X的体积分数减小,故C错误;
D、反应是放热反应,降低温度,反应速率减小,平衡正向进行,Y的转化率增大,故D正确;
故选C.
点评:本题考查了化学平衡的影响因素分析判断,平衡常数、转化率、平衡浓度的计算分析,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
下列物质:①硫化钠溶液、②熟石膏、③碳酸钠晶体、④镁条、⑤漂白粉、⑥硫黄,暴露于空气中而不变质的有( )
| A、①、③ | B、②、⑤ |
| C、④、⑥ | D、③、④ |
下列关于电解质溶液的叙述正确的是( )
| A、常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Clˉ)>c(NH4+)>c(H+)=c(OHˉ) | ||
| B、在0.1mol?L-1 的NaHA溶液pH=4,则H2A为强酸 | ||
| C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊呈红色 | ||
D、向0.1mol?L-1的氨水中加少量硫酸铵固体,则溶液中
|
现有CuO和Fe3O4的混合物7.6g,向其中加入1mol.L-l的H2SO4溶液100mL恰好完全反应,若将15.2g该混合物用足量CO还原,充分反应后剩余固体质量为( )
| A、13.6g |
| B、12g |
| C、6g |
| D、3.2 g |
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是C( )
| A、pH=4的醋酸中:c(H+)=4.0mol?L-1 |
| B、pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 |
| C、饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) |
| D、饱和小苏打溶液中:c(Na+)=c(HCO3-) |



 (苯胺,易被氧化)
(苯胺,易被氧化) 有多种同分异构体,写出同时符合下列4个条件它的同分异构体的结构简式:
有多种同分异构体,写出同时符合下列4个条件它的同分异构体的结构简式: 的流程图:
的流程图: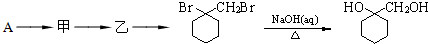 完成甲→乙的化学反应方程式:
完成甲→乙的化学反应方程式:
 为原料
为原料 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: