题目内容
下列对分子性质的解释中,不正确的是( )
| A、碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
B、由于乳酸(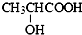 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 |
| C、HF的稳定性很强,是因为其分子间能形成氢键 |
D、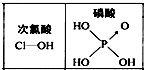 由图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子 |
考点:不同晶体的结构微粒及微粒间作用力的区别,元素周期律的作用,含有氢键的物质
专题:化学键与晶体结构
分析:A.极性分子易溶于极性分子组成的溶剂,非极性分子组成的溶质易溶于非极性分子组成的溶剂;
B.根据手性异构体分子的概念、结构和性质分析;
C.分子稳定性与共价键强度有关;
D.酸性强弱的一条经验规律是:含氧酸分子的结构中含非羟基(羟基为-OH)氧原子数越多,该含氧酸的酸性越强.
B.根据手性异构体分子的概念、结构和性质分析;
C.分子稳定性与共价键强度有关;
D.酸性强弱的一条经验规律是:含氧酸分子的结构中含非羟基(羟基为-OH)氧原子数越多,该含氧酸的酸性越强.
解答:
解:A.碘是非极性分子易溶于非极性溶剂四氯化碳,甲烷属于非极性分子难溶于极性溶剂水,所以都可用相似相溶原理解释,故A正确;
B.碳原子连接四个不同的原子或原子团时,该碳原子为手性碳原子,所以乳酸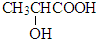 中第二个C为手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子,故B正确;
中第二个C为手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子,故B正确;
C.分子稳定性与共价键强度有,共价键越强,分子越稳定,与氢键无关,氢键决定分子的物理性质,故C错误;
D.H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数,所以磷酸的酸性大于次氯酸,故D正确;
故选:C.
B.碳原子连接四个不同的原子或原子团时,该碳原子为手性碳原子,所以乳酸
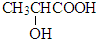 中第二个C为手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子,故B正确;
中第二个C为手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子,故B正确;C.分子稳定性与共价键强度有,共价键越强,分子越稳定,与氢键无关,氢键决定分子的物理性质,故C错误;
D.H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数,所以磷酸的酸性大于次氯酸,故D正确;
故选:C.
点评:本题考查了氢键、手性碳原子、分子稳定性的判断等知识点,题目难度不大,注意手性碳原子的判断方法:碳原子连接四个不同的原子或原子团时,该碳原子为手性碳原子.

练习册系列答案
相关题目
在污染环境的有害气体中,主要由于跟血红蛋白结合而引起中毒的有毒气体是( )
| A、SO2 |
| B、CO2 |
| C、NO2 |
| D、CO |
被誉为“光纤之父”的科学家高锟荣获2009年诺贝尔化学奖.下列叙述不正确的是( )
| A、SiO2是生产光导纤维和粗硅的主要原料 |
| B、工艺师利用盐酸刻蚀石英制作艺术品 |
| C、SiO2与CO2都属于酸性氧化物,都不能与酸反应 |
| D、水晶的主要成分是SiO2 |
下列物质属于弱电解质的是 ( )
| A、氯化钠 | B、蔗糖 |
| C、醋酸 | D、水玻璃 |
已知热化学方程式:SO2(g)+
O2(g)?SO3(g)△H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
| 1 |
| 2 |
| A、等于196.64kJ?mol-1 |
| B、等于196.64 kJ |
| C、小于196.64kJ |
| D、大于196.64kJ |
用NA表示阿佛加德罗常数,下列说法正确的是( )
| A、标准状态下22.4LSO3分子数为NA |
| B、常温常压下,16gO2和16gO3中所含原子数均为NA |
| C、7.8 g Na2O2含有的阴离子数是0.2NA |
| D、1L2mol?L-1的Al(NO3)3溶液中含Al3+个数为2NA |
下列说法正确的是( )
| A、在常温常压下,11.2LN2含有分子数为0.5NA |
| B、在常温常压下,22.4LNe含有原子数为NA |
| C、71gCl2所含有的原子数为2NA |
| D、在同温同压下,相同体积的气体单质含有原子数相同 |
下列说法中正确的是( )
| A、32gO3所含有的原子数目与1molO2所含原子物质的量相等 |
| B、4g金属钙变成钙离子时失去的电子数目为0.1NA |
| C、1molCH3+所含的电子数为10NA |
| D、标准状况下,22.4L H2O所含的分子数为NA |