题目内容
12.下列反应中既属于分解反应又属于氧化还原反应的是( )| A. | Fe+2HCl═FeCl2+H2 | B. | CH4$\frac{\underline{\;高温\;}}{\;}$C+2H2 | ||
| C. | Mg(OH)2+2HCl═MgCl2+2H2O | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2 |
分析 含元素化合价变化的反应为氧化还原反应,一种物质分解生成多种物质的反应为分解反应,以此来解答.
解答 解:A、Fe、H元素的化合价变化,为氧化还原反应,且属于置换反应,故A不选;
B.C、H元素的化合价变化,为氧化还原反应,且属于分解反应,故B选;
C.为复分解反应,无元素的化合价变化,为非氧化还原反应,故C不选;
D.为分解反应,无元素的化合价变化,为非氧化还原反应,故D不选;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化、反应类型为解答的关键,侧重分析与应用能力的考查,注意反应的分类法,题目难度不大.

练习册系列答案
相关题目
2.下列说法正确的是( )
| A. | 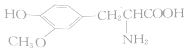 与 与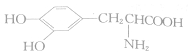 互为同系物 互为同系物 | |
| B. | CH3CH=CHCH3分子中所有原子在同一平面上 | |
| C. | 按系统命名法,化合物 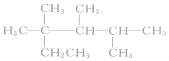 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. | 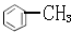 的一溴代物和 的一溴代物和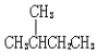 的一溴代物都有4种(不考虑立体结构) 的一溴代物都有4种(不考虑立体结构) |
3.下列离子方程式中,错误的是( )
| A. | 氯气与烧碱溶液反应:Cl2+2OH-=Cl-+ClO-+H2O | |
| B. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ | |
| C. | 二氧化硅与强碱反应:SiO2+2OH-═SiO32-+H2O | |
| D. | 二氧化氮与水反应:3NO2+H2O═2H++2NO3-+NO |
4.下列装置或操作正确并能达到实验目的( )
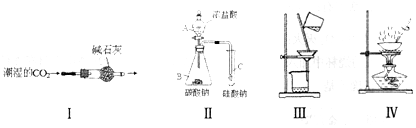

| A. | 用Ⅰ图装置,可得到干燥的CO2 | |
| B. | 用Ⅱ图装置,若C中出现白色沉淀,则可说明H2CO3的酸性强于H2SiO3 | |
| C. | 用Ⅲ图装置,可除去氯化钠溶液中的泥沙 | |
| D. | 用Ⅳ图装置,分离乙醇和水 |
4.下列各组物质熔点高低的比较,正确的是( )
| A. | 晶体硅>金刚石>碳化硅 | B. | CsCl>KCl>NaCl | ||
| C. | SiO2>CO2>He | D. | Br2>I2>He |
5.实验室可以用来直接加热的玻璃仪器是( )
| A. | 小试管 | B. | 容量瓶 | C. | 量筒 | D. | 蒸发皿 |
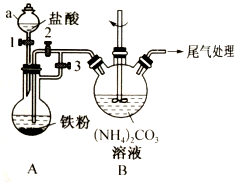 乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得.以下是一种制备乳酸亚铁的实验方法.
乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得.以下是一种制备乳酸亚铁的实验方法.