题目内容
7.对于以aA(g)+bB(g)?cC(g)为例.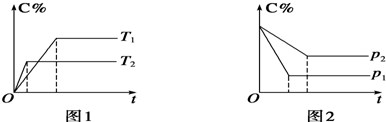
根据图象回答下列问题:
(1)图1中,温度T1、T2的大小关系是T2>T1,温度升高,C%(C的含量)减小,化学平衡逆向移动,正反应是放热反应.
(2)图2中,压强p1、p2的大小关系是P1>P2,压强增大,C%(C的含量)减小,化学平衡逆向移动,a+b<c.
分析 (1)当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短,由图象(1)可知T2>T1,温度越高,平衡时C%越小,说明平衡向逆反应方向移动;
(2)当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短,由图(2)可知P1>P2,压强越大,平衡时C%越小,说明平衡向逆反应方向移动.
解答 解:(1)当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短,由图象(1)可知T2>T1,
温度升高,C%(C的含量)减小,说明平衡逆向移动,故此反应的正反应为放热反应,
故答案为:T2>T1;减小;逆向;放热;
(2)当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短,由图(2)可知P1>P2,压强增大,C%(C的含量)减小,化学平衡逆向移动,则a+b<c,
故答案为:P1>P2;减小;逆向;<.
点评 本题考查化学平衡图象问题,注意根据“先拐先平数值大”原则判断温度、压强大小,再根据C的含量变化判断平衡移动,题目难度不大.

练习册系列答案
相关题目
18.将两种硫酸盐按一定比例混合后共熔,可制得化合物X,X溶于水能电离出K+、Cr3+、SO42-,若将2.83g X中的Cr3+全部氧化为Cr2O72-后,溶液中的Cr2O72-可和过量KI溶液反应,得到3.81g I2,反应的离子方程式为:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,若向溶有2.83g X的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀.由此可推断出X的化学式为( )
| A. | K2SO4•2Cr2(SO4)3 | B. | 2K2SO4•Cr2(SO4)3 | C. | K2SO4•Cr2(SO4)3 | D. | K2SO4•$\frac{1}{2}$Cr2(SO4)3 |
15.下列变化过程中,化学键没有被破坏的是( )
| A. | HCl溶于水 | B. | 干冰升华 | ||
| C. | 固体NaCl熔融 | D. | 煤矿中瓦斯(主要成分CH4)遇火爆炸 |
2.(1)为进行Ⅰ项中的除杂实验(括号内为杂质),请从Ⅱ项中选出一种试剂,从Ⅲ项中选出一合适的实验操作方法分离,将标号填在后面的答案栏内.
(2)a.在洁净的试管中加入少量硝酸银溶液,再逐滴滴加稀氨水,现象是先生成白色沉淀,反应的离子方程式是①Ag++NH3•H2O=AgOH↓+NH4+;继续滴加至沉淀恰好溶解,即得银氨溶液,反应的离子方程式为②AgOH+2NH3=[Ag(NH3)2]++OH-;
b.向a中所得的银氨溶液中滴入少量葡萄糖溶液,混合均匀后,放在水浴中加热3min~5min,即可在试管内壁上形成银镜,则此反应的化学方程式为(葡萄糖的结构简式用G-CHO表示):③G-CHO+2Ag(NH3)2OH$\stackrel{△}{→}$G-COONH4+2Ag↓+3NH3+H2O.
| Ⅰ除杂实验 | Ⅱ试剂 | Ⅲ操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯酚) | A.饱和Na2CO3溶液 B.NaCl晶体 C.NaOH溶液 D.CaO | a.蒸馏 b.分液 c.盐析、过滤 d.萃取 | ① | ||
| ②乙醇(水) | ② | ||||
| ③肥皂(甘油、水) | ③ | ||||
| ④乙酸乙酯(乙酸) | ④ | ||||
b.向a中所得的银氨溶液中滴入少量葡萄糖溶液,混合均匀后,放在水浴中加热3min~5min,即可在试管内壁上形成银镜,则此反应的化学方程式为(葡萄糖的结构简式用G-CHO表示):③G-CHO+2Ag(NH3)2OH$\stackrel{△}{→}$G-COONH4+2Ag↓+3NH3+H2O.
12.下列说法正确的是( )
| A. | 在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 | |
| B. | 根据原子核外电子排布的特点,Cu属于s区元素 | |
| C. | 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 | |
| D. | 核外电子排布由1s22s22p63s1-→1s22s22p6 的变化需要吸收能量 |
19.短周期中三种元素X、Y、Z在周期表中的位置如图,下列有关这三种元素的叙述正确的是( )
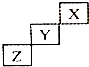

| A. | X是种活泼的非金属元素 | |
| B. | Z的最高价氧化物的水化物是一种弱酸 | |
| C. | Y的氢化物很稳定 | |
| D. | Y元素的最高化合物为+7价 |
16.可以将六种无色液体:C2H5OH、AgNO3溶液,C2H5Br、KI溶液,C6H5OH溶液,C6H6 区分开的试剂是( )
| A. | FeCl3溶液 | B. | 溴水 | ||
| C. | 酸性高锰酸钾溶液 | D. | NaOH溶液 |
17.下列化学用语表示正确的是( )
| A. | 铝原子的结构示意图: | B. | 乙炔的比例模型: | ||
| C. | 水分子的电子式: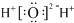 | D. | 硝基苯的结构简式: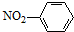 |

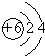 ;元素②的最高价氧化物结构式为:O=C=0;
;元素②的最高价氧化物结构式为:O=C=0;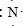 →
→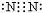 .
.