题目内容
1.某化合物6.4克在氧气中完全燃烧,只生成8.8克CO2和7.2gH2O.下列说法正确的是( )| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳氢原子个数比为1:2 | ||
| C. | 该化合约中一定含有氧元素 | D. | 若要确定其分子式一定需要质谱仪 |
分析 化合物燃烧生成8.8gCO2和7.2gH2O,根据元素守恒则一定含有C、H元素,根据n=$\frac{m}{M}$计算二氧化碳、水的物质的量,进而计算有机物中C、H原子数目之比,根据m=nM计算C、H元素质量,根据质量守恒定律计算判断化合物中是否含有O元素,以此解答该题.
解答 解:化合物燃烧生成8.8gCO2和7.2gH2O,根据元素守恒则一定含有C、H元素,
8.8g二氧化碳的物质的量为:n(CO2)=$\frac{8.8g}{44g/mol}$=0.2mol,n(C)=n(CO2)=0.2mol,m(C)=0.2mol×12g/mol=2.4g,
7.2g水的物质的量为:n(H2O)=$\frac{7.2g}{18g/mol}$=0.4mol,n(H)=2n(H2O)=0.8mol,m(H)=0.8g,
故化合物中N(C):N(H)=0.2mol:0.4mol×2=1:4,
由于m(C)+m(H)=2.4g+0.8g=3.2g<6.4g,所以该化合物中一定含有氧元素,且n(O)=0.2mol,
可知分子式为N(C):N(H):N(O)=0.2mol:0.4mol×2:0.2mol=1:4:1,因C原子化合价已经达到饱和,则不用质谱仪可确定分子式为CH4O,ABD错误,C正确,
故选C.
点评 本题考查有机物组成的确定,为高频考点,侧重考查质量守恒定律,题目难度不大,注意根据质量守恒判断是否含有氧元素.

练习册系列答案
相关题目
11.下列实验方案设计不能达到预期目的是( )
| A. | 向氯酸钾溶液中加入硝酸银溶液和稀硝酸,检验氯酸钾中的氯元素 | |
| B. | 铜可溶于浓硫酸却不溶于稀硫酸,证明浓硫酸的氧化性更强 | |
| C. | 氢氧化铝能分别跟强酸和强碱反应,说明氢氧化铝是两性氢氧化物 | |
| D. | 通过测溶液的pH,鉴别NH4Cl、NaCl、K2CO3三种溶液 |
12.下列表达式正确的是( )
| A. | 甲烷的结构式 CH4 | B. | 乙烯的结构式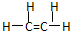 | ||
| C. | 乙烯的结构简式C2H4 | D. | 四氯化碳的电子式: |
9.把Ba(OH)2溶液滴入明矾溶液中,使SO42ˉ全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( )
| A. | AlO2ˉ | B. | Al3+ | C. | Al(OH)3 | D. | Al3+和Al(OH)3 |
16.2011年4月,日本大地震引发的福岛第一核电站核泄漏事故,造成放射性物质碘-131和铯137(${\;}_{55}^{137}Cs$)向外界泄漏.下列相关说法错误的是( )
| A. | 每个${\;}_{55}^{137}Cs$原子中有82个中子 | |
| B. | CsOH的碱性比KOH强 | |
| C. | KIO3是碘的最高价氧化物的水化物的盐 | |
| D. | HI比HF还原性强 |
6.如表是部分短周期元素的原子半径和主要化合价.
用化学用语回答:
(1)Z元素在周期表中的位置第三周期VIIA族.
(2)表格中是否含有短周期主族元素原子半径最大的元素是(填“是”或“否”).
(3)X和Y可以形成18e-化合物,其电子式 .
.
(4)Q元素的原子结构示意图 .
.
( 5 ) Y、M分别形成的常见氢化物沸点H2O>H2S;原因是水分子中含有氢键,故沸点高于硫化氢.
| 元素代号 | X | Y | Z | W | M | Q |
| 原子半径/nm | 0.037 | 0.074 | 0.099 | 0.186 | 0.102 | 0.143 |
| 主要化合价 | +1 | -2 | -1、+7 | +1 | -2、+6 | +3 |
(1)Z元素在周期表中的位置第三周期VIIA族.
(2)表格中是否含有短周期主族元素原子半径最大的元素是(填“是”或“否”).
(3)X和Y可以形成18e-化合物,其电子式
 .
.(4)Q元素的原子结构示意图
 .
.( 5 ) Y、M分别形成的常见氢化物沸点H2O>H2S;原因是水分子中含有氢键,故沸点高于硫化氢.
13.下列实验中,可以加快反应速率的是( )
| A. | 钠与水反应时,增加水的量 | |
| B. | 锌与稀硫酸反应时,加入少量CuSO4固体 | |
| C. | 用18mol/L的硫酸溶液代替2m0l/L硫酸溶.液常温下与铝反应 | |
| D. | 锌与稀硫酸反应时,加入少量醋酸钠固体 |
10.下列说法正确的是( )
| A. | 用酸性重铬酸钾溶液检验酒驾,是因为乙醇被还原 | |
| B. | 酸性高锰酸钾溶液和溴水都既能鉴别出甲烷和乙烯又能除去甲烷中含有的乙烯再经干燥而获得纯净的甲烷 | |
| C. | 石油中含有C5~C11的烷烃,可以通过分馏得到汽油 | |
| D. | 煤中含有苯和甲苯,可以用先干馏,后蒸馏的方法把它们分离出来 |
10.1g碳与适量水蒸气反应生成CO和H2,需吸收10.94kJ热量,此反应的热化学方程式为( )
| A. | C+H2O═CO+H2 △H=+131.3 kJ•mol-1 | |
| B. | C(s)+H2O(g)═CO(g)+H2(g)△H=+10.94 kJ•mol-1 | |
| C. | C(s)+H2O(l)═CO(g)+H2(g)△H=+131.3 kJ•mol-1 | |
| D. | C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3 kJ•mol-1 |