题目内容
某同学组装如图所示电化学装置,电极I为Zn,其它电极均为Cu.下列说法错误的是( )

| A、电极I发生氧化反应 |
| B、相同的时间内,电极Ⅱ与Ⅳ质量变化相同 |
| C、电极Ⅲ的电极反应:4OH--4e-=2H2O+O2↑ |
D、电流方向:电极Ⅳ→ →电极I →电极I |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电极Ⅰ为Zn,其它均为Cu,Zn易失电子作负极,所以Ⅰ是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,电子方向从负极流向正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,据此分析解答.
解答:
解:电极Ⅰ为Zn,其它均为Cu,Zn易失电子作负极,所以Ⅰ是负极、Ⅳ是阴极,Ⅲ是阳极、Ⅱ是正极,
A.电极Ⅰ上电极上为Zn失电子,发生氧化反应,故A正确;
B、电极II是正极,电极反应:Cu 2++2e-=Cu;电极Ⅳ是阴极,该电极上发生反应为Cu 2++2e-=Cu,由于流经各个电极的电子的量相同,故两个电极的质量变化相同,故B正确;
C、电极Ⅲ为阳极,电极反应式为Cu-2e-═Cu2+,故C错误;
D、电子方向从负极流向正极,即电极Ⅰ→电极Ⅳ,而电流方向与电子的方向相反,故电流的流向为:电极Ⅳ→ →电极I,故D正确;
→电极I,故D正确;
故选C.
A.电极Ⅰ上电极上为Zn失电子,发生氧化反应,故A正确;
B、电极II是正极,电极反应:Cu 2++2e-=Cu;电极Ⅳ是阴极,该电极上发生反应为Cu 2++2e-=Cu,由于流经各个电极的电子的量相同,故两个电极的质量变化相同,故B正确;
C、电极Ⅲ为阳极,电极反应式为Cu-2e-═Cu2+,故C错误;
D、电子方向从负极流向正极,即电极Ⅰ→电极Ⅳ,而电流方向与电子的方向相反,故电流的流向为:电极Ⅳ→
 →电极I,故D正确;
→电极I,故D正确;故选C.
点评:本题考查了原电池原理,正确判断正负极是解本题关键,再结合各个电极上发生的反应来分析解答,题目难度中等.

练习册系列答案
相关题目
下列化合物中同分异构体数目最少的是( )
| A、丁烷 | B、戊醇 |
| C、戊烯 | D、二溴丙烷 |
下列叙述正确的是( )
| A、利用惰性电极电解饱和食盐水的过程中,溶液中水的电离平衡向左移动 |
| B、溴元素和碘元素被称为“海洋元素” |
| C、向AlCl3溶液中加入氨水可制取Al(OH)3 |
| D、Fe分别与氯气和稀盐酸反应可得到同一种氯化物 |
铅蓄电池的总反应式为:PbO2+Pb+2H2SO4
2PbSO4+2H2O,据此判断下列叙述正确的是( )
| 充电 |
| 放电 |
| A、放电时,H2SO4 浓度增加 |
| B、放电时,负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C、在充电时,电池中每转移1mol电子,理论上生成1mol硫酸 |
| D、在充电时,阴极发生的反应是PbSO4-2e-+2H2O=PbO2+SO2-4+4H+ |
有一种纸质软电池,该电池采用薄层 纸片作为载体和传导体,一面附着锌,另一面附着二氧化锰.电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH),关于此电池,下列说法中正确的是( )
| A、该电池Zn为负极,ZnO为正极,MnO2催化剂 |
| B、该电池的正极反应为MnO2+e+H2O=MnO(OH)+OH |
| C、放电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| D、电池工作时OH通过薄层纸片向附着二氧化锰的电极移动 |
在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象.可以通过下列装置所示实验进行探究.下列说法正确的是( )
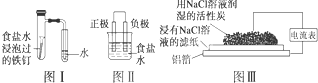

| A、按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管 |
| B、图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁 |
| C、铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-═Cl2↑ |
| D、图Ⅲ装置的总反应为4Al+3O2+6H2O═4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑 |
下列关于氧化还原反应的描述正确的是( )
| A、离子反应一定是氧化还原反应 |
| B、阴离子只有还原性 |
| C、阳离子只有氧化性 |
| D、反应2H2S+SO2=3S+2H2O中氧化产物与还原产物物质的量之比为2:1 |
完全燃烧0.1mol某芳香烃后得到44gCO2 和12.6gH2O,若不考虑立体异构,则该芳香烃可能的结构共有( )
| A、4种 | B、13种 |
| C、22种 | D、26种 |