题目内容
对气体反应:mA+nB?eC 温度(T)、压强(P)、时间(t)与生成物的体积百分数C%的关系图,下列结论正确的是( )


| A、正反应是放热反应 |
| B、m+n<e |
| C、T3>T4 |
| D、T1>T2 |
考点:体积百分含量随温度、压强变化曲线
专题:
分析:根据“先拐先平数值大”知,温度T1<T2,升高温度,C的含量减小,说明平衡向逆反应方向移动,则正反应是放热反应;根据右图知,同一温度下,增大压强,C的含量增大,说明平衡向正反应方向移动,则正反应是气体体积减小的反应,据此分析解答.
解答:
解:A.左图中根据“先拐先平数值大”知,温度T1<T2,升高温度,C的含量减小,说明平衡向逆反应方向移动,则正反应是放热反应,故A正确;
B.根据右图知,同一温度下,增大压强,C的含量增大,说明平衡向正反应方向移动,则正反应是气体体积减小的反应,所以m+n>e,故B错误;
C.根据右图知,同一压强下,C的百分含量T3>T4,该反应的正反应是放热反应,降低温度平衡向正反应方向移动,C的百分含量增大,所以温度T3<T4,故C错误;
D.根据A知,温度T1<T2,故D错误;
故选A.
B.根据右图知,同一温度下,增大压强,C的含量增大,说明平衡向正反应方向移动,则正反应是气体体积减小的反应,所以m+n>e,故B错误;
C.根据右图知,同一压强下,C的百分含量T3>T4,该反应的正反应是放热反应,降低温度平衡向正反应方向移动,C的百分含量增大,所以温度T3<T4,故C错误;
D.根据A知,温度T1<T2,故D错误;
故选A.
点评:本题考查温度、压强对化学平衡的影响,采用“先拐先平数值大”、“定一议二”的方法解答即可,题目难度中等.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2═2Fe(OH)2.以下说法正确的是( )
| A、负极发生的反应为:Fe-2e-=Fe2+ |
| B、正极发生的反应为:4OH--4e-═2H2O+O2↑ |
| C、原电池是将电能转变为化学能的装置 |
| D、钢柱在水下部分比在空气与水交界处更容易腐蚀 |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、欲配制1.00 L 1.00 mol?L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| B、1 mol Cl2与足量的铁反应,转移的电子数为3NA |
| C、0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10 NA |
| D、标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为2NA |
下列离子方程式书写正确的是( )
| A、铝粉投入氢氧化钠溶液中:2Al+2OH-═2AlO2-+H2↑ |
| B、氯化铝溶液中加入足量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| C、氯化铁溶液中加入铁粉:Fe3++Fe═2Fe2+ |
| D、氯化亚铁溶液跟氯气反应:Fe2++Cl2═Fe3++2Cl- |
下列反应的离子方程式正确的是( )
| A、溴化亚铁溶液中通入过量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
| B、草酸和少量烧碱溶液:H2C2O4+2OH-═C2O42-+2H2O |
| C、漂白粉溶液吸收过量的二氧化碳:ClO-+H2O+CO2═HClO+HCO3- |
| D、将铜片投入足量稀硝酸:Cu+NO3-+4H+═Cu2++NO↑+2H2O |
猪流感是一种由甲型流感病毒的一种亚型引起的传染性疾病综合症,被国际兽疫局设为A类传染病,又称真性鸡瘟或欧洲鸡瘟.禽流感病毒对常用消毒剂十分敏感,容易将其杀灭.下列不能杀灭禽流感病毒的方法或物质的是( )
| A、高温蒸煮 | B、用纯净水多次洗涤 |
| C、双氧水 | D、过氧乙酸 |
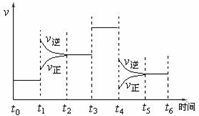 某一容积可变的密闭体系中发生下列反应:N2(g)+3H2(g)?2NH3(g)△H<0,回答下列问题:
某一容积可变的密闭体系中发生下列反应:N2(g)+3H2(g)?2NH3(g)△H<0,回答下列问题: