题目内容
 某一容积可变的密闭体系中发生下列反应:N2(g)+3H2(g)?2NH3(g)△H<0,回答下列问题:
某一容积可变的密闭体系中发生下列反应:N2(g)+3H2(g)?2NH3(g)△H<0,回答下列问题:(1)对于合成氨工业生产条件的选择,下列说法正确的是(选填字母序号)
A.温度、压强越大,越有利于化学平衡的正向移动;
B.铁触媒在该温度时活性大;
C.工业生产受动力、材料、设备等条件的限制;
D.使用催化剂有利于提高反应的转化率.
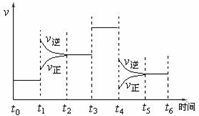
(2)如图是某一时间段中反应速率与反应进程的关系图:①处于平衡状态的时间段是
②在t1、t3、t4时刻,体系中分别是何种条件发生了什么样变化?t1:
a.t0~t1b.t2~t3 c.t3~t4 d.t5~t6.
考点:化学反应速率变化曲线及其应用,合成氨条件的选择
专题:
分析:(1)A.温度越高平衡逆向进行,不利于化学平衡的正向移动,压强越大平衡正向进行,越有利于化学平衡的正向移动;
B.铁触媒在该温度时活性大,有利于提高反应速率;
C.工业生产受动力、材料、设备等条件的限制,压强温度改变要求设备高;
D.使用催化剂改变反应速率,不改变化学平衡;
(2)①反应达到平衡状态,正逆反应速率相同;
②由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动;
③由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动,均使氨气的含量减.
B.铁触媒在该温度时活性大,有利于提高反应速率;
C.工业生产受动力、材料、设备等条件的限制,压强温度改变要求设备高;
D.使用催化剂改变反应速率,不改变化学平衡;
(2)①反应达到平衡状态,正逆反应速率相同;
②由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动;
③由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动,均使氨气的含量减.
解答:
解:由N2(g)+3H2(g)?2NH3(g)△H<0,可知,该反应为放热反应,且为气体体积减小的反应,则
(1)A.温度越高平衡逆向进行,不利于化学平衡的正向移动,压强越大平衡正向进行,越有利于化学平衡的正向移动,故A错误;
B.铁触媒在该温度时活性大,有利于提高反应速率,故B正确;
C.工业生产受动力、材料、设备等条件的限制,压强温度改变要求设备高,故B正确;
D.使用催化剂改变反应速率,不改变反应的转化率,故D错误;
故答案为:BC;
(2)①反应达到平衡状态,正逆反应速率相同,说明反应达到平衡状态,图象分析可知达到平衡状态时间段为:t0~t1 t2~t3 t3~t4 t5~t6;
故答案为:t0~t1、t2~t3、t3~t4、t5~t6;
②由图可知,t1正逆反应速率均增大,且逆反应速率大于正反应速率,改变条件应为升高温度;
t3正逆反应速率同等程度的增大,改变条件应为使用催化剂;
t4时正逆反应速率均减小,且逆反应速率大于正反应速率,改变条件应为减小压强,
故答案为:升高温度;使用催化剂;减小压强;
③由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动,均使氨气的含量减少,则t0~t1氨气的含量最大,
故答案为:a.
(1)A.温度越高平衡逆向进行,不利于化学平衡的正向移动,压强越大平衡正向进行,越有利于化学平衡的正向移动,故A错误;
B.铁触媒在该温度时活性大,有利于提高反应速率,故B正确;
C.工业生产受动力、材料、设备等条件的限制,压强温度改变要求设备高,故B正确;
D.使用催化剂改变反应速率,不改变反应的转化率,故D错误;
故答案为:BC;
(2)①反应达到平衡状态,正逆反应速率相同,说明反应达到平衡状态,图象分析可知达到平衡状态时间段为:t0~t1 t2~t3 t3~t4 t5~t6;
故答案为:t0~t1、t2~t3、t3~t4、t5~t6;
②由图可知,t1正逆反应速率均增大,且逆反应速率大于正反应速率,改变条件应为升高温度;
t3正逆反应速率同等程度的增大,改变条件应为使用催化剂;
t4时正逆反应速率均减小,且逆反应速率大于正反应速率,改变条件应为减小压强,
故答案为:升高温度;使用催化剂;减小压强;
③由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动,均使氨气的含量减少,则t0~t1氨气的含量最大,
故答案为:a.
点评:本题考查影响化学反应速率的因素,注意把握反应的特点及图象分析是解答的关键,明确温度、压强、催化剂对反应速率的影响即可解答,题目难度不大.

练习册系列答案
相关题目
下列各实验现象正确的是( )
| A、苯和乙烯都能使溴水因加成反应而褪色 |
| B、稀硫酸中加入铜粉不反应,再加入硝酸钠,铜粉溶解 |
| C、乙酸乙酯与新制的氢氧化铜悬浊液共热,产生红色沉淀 |
| D、将CO2通入氯化钡溶液中产生白色沉淀 |
下列各物质间能发生置换反应的是( )
| A、氯气通入碘化钾溶液中 |
| B、碘水加入溴化钠溶液中 |
| C、溴水加入氯化钠溶液中 |
| D、碘水加入氯化钠溶液中 |
下列说法正确的是( )
| A、6.02×1023个碳原子就是阿伏加德罗常数 |
| B、1mol氧就是6.02×1023个氧分子. |
| C、1molNa失去1mol电子生成1molNa+ |
| D、摩尔是七个基本物理量之一 |
对气体反应:mA+nB?eC 温度(T)、压强(P)、时间(t)与生成物的体积百分数C%的关系图,下列结论正确的是( )


| A、正反应是放热反应 |
| B、m+n<e |
| C、T3>T4 |
| D、T1>T2 |
1mol/L硫酸溶液的含义是( )
| A、1L水中含有1mol硫酸 |
| B、1L溶液中含1molH+ |
| C、将98g硫酸溶于1L水所配成的溶液 |
| D、1L溶液中含有1mol硫酸 |
水体污染物有:Ⅰ含盐酸的酸性废水,Ⅱ油类、氰化物、硫化物,Ⅲ重金属离子;污水处理的化学方法有:a中和法,b氧化还原法,c沉淀法.所采用的方法对水体污染物处理不正确的是( )
| A、Ⅰa | B、Ⅰb | C、Ⅱb | D、Ⅲc |
 X、Y、Z、Q均为短周期元素,它们在周期表中相对位置如图所示.若X原子的
X、Y、Z、Q均为短周期元素,它们在周期表中相对位置如图所示.若X原子的最外层电子是内层电子数的2倍.下列说法中,正确的是( )
| A、X与Q的化合物中含有共价键 |
| B、最高价氧化物对应水化物的酸性:Q比Z弱 |
| C、14X和14Y具有相同的质量数,互为同位素 |
| D、Q与Fe反应生成的化合物中,铁元素显+3价 |