题目内容
下列说法正确的是( )
| A、维生素C有较强的还原性,可将I2、Fe3+还原 |
| B、使用青霉素时,不用进行皮试可直接静脉注射 |
| C、酒精、双氧水、次氯酸、臭氧均可用于餐具杀菌消毒 |
| D、胃酸过多的病人都可以服用氢氧化钠、氢氧化铝、碳酸钠等中和胃酸的药 |
考点:人体必需的维生素的主要来源及其摄入途径,药物的主要成分和疗效
专题:化学应用
分析:A.维生素C有较强的还原性;
B.青霉素可能引起过敏反应;
C.酒精、双氧水、次氯酸、臭氧都能使蛋白质发生变性;
D.氢氧化钠有腐蚀性.
B.青霉素可能引起过敏反应;
C.酒精、双氧水、次氯酸、臭氧都能使蛋白质发生变性;
D.氢氧化钠有腐蚀性.
解答:
解:A.维生素C有较强的还原性,可将I2、Fe3+还原,故A正确;
B.青霉素可能引起过敏反应,需要先做皮试,故B错误;
C.酒精、双氧水、次氯酸、臭氧都能使蛋白质发生变性,杀菌消毒,故C正确;
D.氢氧化钠有腐蚀性,碳酸钠碱性较强,不能用于治疗胃酸过多,故D错误.
故选AC.
B.青霉素可能引起过敏反应,需要先做皮试,故B错误;
C.酒精、双氧水、次氯酸、臭氧都能使蛋白质发生变性,杀菌消毒,故C正确;
D.氢氧化钠有腐蚀性,碳酸钠碱性较强,不能用于治疗胃酸过多,故D错误.
故选AC.
点评:本题考查药物的主要成分和疗效,难度不大,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
浓H2SO4 密度1.84g/mL,物质的量浓度为18.4mol/L,质量分数为98%,取10mL浓H2SO4和amL水混合得物质的量浓度为Cmol/L,质量分数为b%.下列组合正确的是( )
(1)若b=49 则a=18.4 C>9.2 (2)若b=49 则a=18.4 C<9.2
(3)若C=9.2 则a>10 b>49% (4)若C=9.2 则a>10 b<49%
(1)若b=49 则a=18.4 C>9.2 (2)若b=49 则a=18.4 C<9.2
(3)若C=9.2 则a>10 b>49% (4)若C=9.2 则a>10 b<49%
| A、(1)(3) |
| B、(1)(4) |
| C、(2)(3) |
| D、(2)(4) |
下列离子方程式正确的是( )
| A、稀硝酸中加入过量铁粉:Fe+NO3-+4 H+═Fe3++NO↑+2 H2O |
| B、向碘化亚铁溶液中通少量氯气:Cl2+2Fe2+═2Fe3++2Cl- |
| C、工业刻蚀印刷电路板:2 Fe3++Cu═2 Fe2++Cu2+ |
| D、氢氧化铁溶于氢碘酸:Fe(OH)3+3 H+═Fe3++3 H2O |
向CH3COOH溶液中加水,下列各项增大的是( )
| A、c(CH3COO-) |
| B、c(H+) |
| C、Kw |
| D、pH |
某同学写出的下列烷烃的名称中,不正确的是( )
| A、3-甲基-2-乙基戊烷 |
| B、3,3-二甲基己烷 |
| C、2,3-二甲基丁烷 |
| D、2,2,3,3-四甲基丁烷 |
一定质量的氧气中含有1mole-,则氧气的质量是( )
| A、2g | B、4g |
| C、16g | D、32g |
下列说法正确的是( )
A、按系统命名法命名时,图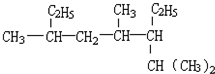 的名称是3,5,7-三甲基-6-乙基辛烷 的名称是3,5,7-三甲基-6-乙基辛烷 |
B、有机物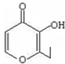 的一种芳香族同分异构体能发生银镜反应 的一种芳香族同分异构体能发生银镜反应 |
| C、等质量的乙酸甲酯和甲酸乙酯完全燃烧生成水的量相等 |
D、高分子化合物 ,其单体为对苯二甲酸和乙醇 ,其单体为对苯二甲酸和乙醇 |
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g),达到平衡时,测的A的浓度为0.5mol/L,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测的A的浓度降低为0.3mol/L,下列有关判断正确的是( )
| A、x+y<z |
| B、平衡向正反应方向移动 |
| C、C的体积分数下降 |
| D、A的转化率提高 |
下列说法正确的是( )
| A、实验中为了得到纯净的晶体,制得的硫酸亚铁铵和阿司匹林晶体均用酒精洗涤 |
| B、在原电池实验中,加入重铬酸钾溶液或6%H2O2溶液的目的是降低电极的极化作用 |
| C、在盛有氯化钴溶液的试管中,加入一定量的浓盐酸,会使溶液的红色加深 |
| D、在用标准NaOH溶液滴定食醋的实验中,滴定终点读取滴定管刻度时,仰视标准液液面,会使实验误差偏低 |