题目内容
下列离子方程式正确的是( )
| A、稀硝酸中加入过量铁粉:Fe+NO3-+4 H+═Fe3++NO↑+2 H2O |
| B、向碘化亚铁溶液中通少量氯气:Cl2+2Fe2+═2Fe3++2Cl- |
| C、工业刻蚀印刷电路板:2 Fe3++Cu═2 Fe2++Cu2+ |
| D、氢氧化铁溶于氢碘酸:Fe(OH)3+3 H+═Fe3++3 H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成硝酸亚铁、NO和水;
B.碘离子的还原性强,优先被少量氯气氧化;
C.电子、电荷守恒;
D.发生氧化还原反应生成碘化亚铁、碘、水.
B.碘离子的还原性强,优先被少量氯气氧化;
C.电子、电荷守恒;
D.发生氧化还原反应生成碘化亚铁、碘、水.
解答:
解:A.稀硝酸中加入过量铁粉的离子反应为3Fe+2NO3-+8H+═3Fe3++2NO↑+4H2O,故A错误;
B.向碘化亚铁溶液中通少量氯气的离子反应为Cl2+2I-═I2+2Cl-,故B错误;
C.工业刻蚀印刷电路板的离子反应为2Fe3++Cu═2Fe2++Cu2+,故C正确;
D.氢氧化铁溶于氢碘酸的离子反应为2Fe(OH)3+2I-+6H+═2Fe2++I2+6H2O,故D错误;
故选C.
B.向碘化亚铁溶液中通少量氯气的离子反应为Cl2+2I-═I2+2Cl-,故B错误;
C.工业刻蚀印刷电路板的离子反应为2Fe3++Cu═2Fe2++Cu2+,故C正确;
D.氢氧化铁溶于氢碘酸的离子反应为2Fe(OH)3+2I-+6H+═2Fe2++I2+6H2O,故D错误;
故选C.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应考查,综合性较强,题目难度不大.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
只用水不能鉴别的一组物质是( )
| A、乙醇和乙酸 |
| B、乙酸乙酯和乙醇 |
| C、苯和四氯化碳 |
| D、苯和汽油 |
按照物质的树状分类法和交叉分类法,HNO3应属于( )
①酸;②氢化物;③氧化物;④含氧酸;⑤弱酸;⑥化合物;⑦一元酸.
①酸;②氢化物;③氧化物;④含氧酸;⑤弱酸;⑥化合物;⑦一元酸.
| A、①②③④⑥⑦ |
| B、①③⑤⑥⑦ |
| C、①④⑥⑦ |
| D、①④⑤⑥⑦ |
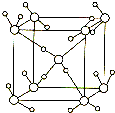 图为冰的一种骨架形式,依此为单位向空间延伸,则x mol冰中含有多少mol氢键( )
图为冰的一种骨架形式,依此为单位向空间延伸,则x mol冰中含有多少mol氢键( )| A、2x | B、4x | C、6x | D、8x |
在下列条件下,能大量共存的微粒组是( )
| 化学式 | 电离常数(25℃) |
| CH3COOH | Ki=1.7×10-5 |
| HClO | Ki=3.0×10-8 |
| H2CO3 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A、c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- |
| B、右表提供的数据下:HClO、HCO3-、ClO-、CO32- |
| C、能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- |
| D、中性的溶液中:CO32-、Na+、SO42-、AlO2- |
下列说法正确的是( )
| A、维生素C有较强的还原性,可将I2、Fe3+还原 |
| B、使用青霉素时,不用进行皮试可直接静脉注射 |
| C、酒精、双氧水、次氯酸、臭氧均可用于餐具杀菌消毒 |
| D、胃酸过多的病人都可以服用氢氧化钠、氢氧化铝、碳酸钠等中和胃酸的药 |
下列各组的两种溶液中,分别加入足量氨水,观察到的现象相同的是( )
| A、FeCl3、AlCl3 |
| B、NaCl、BaCl2 |
| C、MgCl2、CuCl2 |
| D、FeCl2、FeCl3 |