题目内容
4.理论上不能设计为原电池的化学反应是( )| A. | 2C O (g)+O2(g)═2CO2(g) | B. | HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l) | ||
| C. | 2H2(g)+O2(g)═2H2O(l) | D. | Zn(s)+Ag2 O(s)═Zn O(s)+2Ag(s) |
分析 自发的氧化还原反应能设计成原电池,复分解反应不能设计成原电池,根据反应的类型判断.
解答 解:A、2C O (g)+O2(g)═2CO2(g),该反应属于自发的氧化还原反应,所以能设计成原电池,故A不选;
B、HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l),该反应属于复分解反应,不是氧化还原反应,所以不能设计成原电池,故B选;
C、2H2(g)+O2(g)═2H2O(l),该反应属于自发的氧化还原反应,所以能设计成原电池,故C不选;
D、Zn(s)+Ag2 O(s)═Zn O(s)+2Ag(s),该反应属于自发的氧化还原反应,所以能设计成原电池,故D不选;
故选B.
点评 本题考查学生设计成原电池的反应应具备的条件,难度不大,根据原电池的构成条件进行设计原电池即可.

练习册系列答案
相关题目
15.下列说法正确的是( )
| A. | 短周期元素形成离子后,最外层都达到8电子稳定结构 | |
| B. | 检验铵盐方法:加氢氧化钠溶液,加热,用蘸有浓硫酸的玻璃棒靠近瓶口 | |
| C. | .制取硝酸铝方法:用AlCl3溶液和氨水反应,过滤得沉淀,再加稀HNO3 | |
| D. | 等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应,后者放出的CO2多 |
12.下列化学用语表示正确的是( )
| A. | 氯化铵的电子式: | B. | 中子数为18的硫原子:${\;}_{16}^{18}$S | ||
| C. | 水分子的球棍模型: | D. | 乙烯的结构简式:CH2=CH2 |
9.设NA为阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 标准状况下,22.4 L氯气与过量的氢氧化钠溶液完全反应转移的电子数为2 NA | |
| B. | 18gD216O中含有的中子数为9 NA | |
| C. | 标准状况下,22.4L H2O中含有的共用电子对数为2NA | |
| D. | 常温常压下,11.2L的NO2和CO2混合气体含有氧原子数为NA |
16.20℃时,H2S的饱和溶液1L,其浓度为0.1mol/L,若要使溶液的pH增大的同时c(S2-)增大,可采取的措施是( )
| A. | 加入适量的水 | B. | 加入适量的NaOH固体 | ||
| C. | 通入适量的SO2 | D. | 加入适量的CuSO4固体 |
19.下列离子方程式正确的是( )
| A. | 向小苏打溶液中加入甲酸溶液:HCO3-+H+═CO2↑+H2O | |
| B. | 甲酸苯酯与银氨溶液水浴加热的化学方程式: | |
| C. |  在足量烧碱液中水解: 在足量烧碱液中水解: +2OH-→ +2OH-→ +CH3COO-+2H2O +CH3COO-+2H2O | |
| D. | 向C6H5ONa溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
 在5-氨基四唑(
在5-氨基四唑(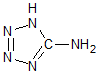 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.


