题目内容
9.设NA为阿伏伽德罗常数的值,下列说法中正确的是( )| A. | 标准状况下,22.4 L氯气与过量的氢氧化钠溶液完全反应转移的电子数为2 NA | |
| B. | 18gD216O中含有的中子数为9 NA | |
| C. | 标准状况下,22.4L H2O中含有的共用电子对数为2NA | |
| D. | 常温常压下,11.2L的NO2和CO2混合气体含有氧原子数为NA |
分析 A、求出氯气的物质的量,然后根据氯气和碱反应的反应是歧化反应来分析;
B、求出重水的物质的量,然后根据重水中含10个中子来分析;
C、标况下水为液体;
D、常温常压下气体摩尔体积大于22.4L/mol.
解答 解:A、标况下22.4L氯气的物质的量为1mol,而氯气和碱反应的反应是歧化反应,故1mol氯气转移1mol电子即NA个,故A错误;
B、18g重水的物质的量为0.9mol,而重水中含10个中子,故0.9mol重水中含9NA个中子,故B正确;
C、标况下水为液体,故不能根据气体摩尔体积来计算其物质的量和共用电子对数,故C错误;
D、常温常压下气体摩尔体积大于22.4L/mol,故11.2L混合气体的物质的量小于0.5mol,则含有的氧原子个数小于NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
19.下列说法正确的是( )
| A. | 按系统命名法,化合物 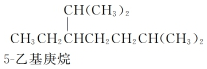 的名称为2,6二甲基5乙基庚烷 的名称为2,6二甲基5乙基庚烷 | |
| B. | 丙氨酸和苯丙氨酸脱水,最多可生成3种二肽 | |
| C. | 化合物  是苯的同系物 是苯的同系物 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
20.氢化铵(NH4H)是一种离子化合物,与氯化铵的结构相似,又知它与水反应有气体生成.下列关于氢化铵叙述不正确的是( )
| A. | 是离子化合物,含有离子键和共价键 | |
| B. | 电子式是: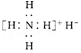 | |
| C. | 与水反应时,氢化铵被氧化 | |
| D. | 固体投入少量的水中,有两种气体产生 |
17.M元素的一个原子失去两个电子转移到R元素的两个原子中去,形成离子化合物.下列四种化合物都符合条件,但从结构上看,有一种物质与其它三种明显不同,该物质是( )
| A. | FeS2 | B. | CaC2 | C. | BaO2 | D. | MgCl2 |
4.理论上不能设计为原电池的化学反应是( )
| A. | 2C O (g)+O2(g)═2CO2(g) | B. | HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l) | ||
| C. | 2H2(g)+O2(g)═2H2O(l) | D. | Zn(s)+Ag2 O(s)═Zn O(s)+2Ag(s) |
14.有一处于平衡状态的反应:X(s)+3Y(g)?2Z(g),△H<0.为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温
②低温
③高压
④低压
⑤加催化剂
⑥分离出Z
⑦增加X
⑧增加Y.
①高温
②低温
③高压
④低压
⑤加催化剂
⑥分离出Z
⑦增加X
⑧增加Y.
| A. | ①③⑤⑦ | B. | ②③⑤⑦ | C. | ②③⑥⑧ | D. | ②④⑥⑧ |
1.下列与有机物的结构、性质有关的叙述正确的是( )
| A. | 苯和乙烯都能使溴水褪色,且反应原理相同 | |
| B. | 乙炔和苯均为不饱和烃,都只能发生加成反应 | |
| C. | 乙烯和氯乙烯都可以通过聚合反应得到高分子材料 | |
| D. | 分别用乙烷和乙烯制备氯乙烷的反应类型完全相同 |
18.下列说法正确的是( )
| A. | N2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| B. | 某物质在熔融态能导电,则该物质中一定含有离子键 | |
| C. | 干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力 | |
| D. | MgF2晶体中的化学键是共价键 |
4.在三个相同体积的密闭容器中分别充入N2、CH4、CO2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
| A. | p(N2)>p(CH4)>p(CO2) | B. | p(CH4)>p(N2)>p(CO2) | C. | p(CH4)>p(CO2)>p(N2) | D. | p(CO2)>p(N2)>p(CH4) |