题目内容
7. 图为北京奥运会的奖牌--“金镶玉”牌,使用了昂贵的玉石材料,其化学成分多为含水钙镁硅酸盐,如Ca2Mg5Si8O22(OH)2等.下列说法正确的是( )
图为北京奥运会的奖牌--“金镶玉”牌,使用了昂贵的玉石材料,其化学成分多为含水钙镁硅酸盐,如Ca2Mg5Si8O22(OH)2等.下列说法正确的是( )| A. | Ca2Mg5Si8O22(OH)2可用氧化物的形式表示为2CaO•5MgO•8SiO2•H2O | |
| B. | 从分类的角度看,Ca2Mg5Si8O22(OH)2为氧化物 | |
| C. | 玉石材料性质稳定,耐强酸和强碱的腐蚀 | |
| D. | Ca2Mg5Si8O22(OH)2易溶于水 |
分析 Ca2Mg5Si8O22(OH)2属于盐类,易被强酸腐蚀,不溶于水,可用氧化物的形式表示为2CaO•5MgO•8SiO2•H2O,氧化物要求只含有两种元素,切其中一种元素是氧元素.
解答 解:A.Ca2Mg5Si8O22(OH)2可用氧化物的形式表示为2CaO•5MgO•8SiO2•H2O,故A正确;
B.氧化物要求只含有两种元素,切其中一种元素是氧元素,Ca2Mg5Si8O22(OH)2属于盐类,故B错误;
C.玉石材料性质稳定,属于盐类易被强酸腐蚀,故C错误;
D.属于盐是硅酸钙、硅酸镁不溶于水,故D错误;
故选A.
点评 本题考查了硅酸盐的组成、性质等知识,注意知识的积累,题目难度不大.

练习册系列答案
相关题目
18.具有“-CH2OH”结构的醇类物质中,能被酸性高锰酸钾溶液氧化成相应的酸.分子式为C5Hl2O可被氧化成酸的醇共有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
2.下列离子方程式中正确的是( )
| A. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 氢氧化钙溶液与碳酸氢镁溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| D. | KI溶液与H2SO4酸化的H2O2溶液混合:2 I-+H2O2+2 H+═2 H2O+I2 |
12.1874年22岁的范特霍夫和27岁的勒贝尔分别提出碳正四面体学说,建立了分子的立体概念.如图所示均能表示甲烷的分子结构,哪一种更能反映其真实存在状况( )
| A. | 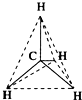 结构示意图 | B. |  电子式 | C. | 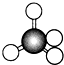 球棍模型 | D. | 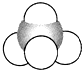 比例模型 |
 ;
;