题目内容
有一块铝铁合金,将其溶解于足量盐酸中,再加入过量NaOH溶液,在空气中静置至红褐色沉淀不再增加时,将沉淀滤出再灼烧至恒重,得到残留物的质量与原合金质量相同,则合金中铝的质量分数( )
| A、22.2% | B、30% |
| C、75.5% | D、80.6% |
考点:有关混合物反应的计算
专题:计算题
分析:铝铁合金粉末溶于足量盐酸中,加入过量NaOH 溶液,沉淀为氢氧化铁,则经洗涤、干燥、灼烧,得到红棕色粉末为氧化铁,氧化铁质量等于合金的质量,利用组成可知氧化铁中氧元素的质量等于合金中铝的质量,以此来解答.
解答:
解:由铝铁合金粉末溶于足量盐酸中,加入过量NaOH 溶液,沉淀为氢氧化铁,则经洗涤、干燥、灼烧,得到红棕色粉末为氧化铁,氧化铁质量等于合金的质量,利用组成可知氧化铁中氧元素的质量等于合金中铝的质量,则合金中Al的质量分数等于氧化铁中氧的质量分数=
×100%=30%,
故选B.
| 16×3 |
| 160 |
故选B.
点评:本题考查混合物的有关计算,侧重于学生的分析能力和计算能力的考查,明确发生的反应找出合金与氧化物的关系是解答本题的关键,注意铁元素的守恒,难度不大.

练习册系列答案
相关题目
家用消毒液发生器是化学知识在日常生活中的“创新”应用.该发生器利用常见的精盐和自来水为反应物.通电时,发生器内电解槽里的极板上产生大量水泡.切断电源后所得的消毒液有强烈的杀菌能力,且对人体无害.溶液中发生的主要的反应为:2NaCl+2H2O
2NaOH+H2+Cl2 2NaOH+Cl2=NaCl+NaClO+H2O则所得消毒液的有效成分是( )
| ||
| A、NaCl |
| B、Cl2 |
| C、NaClO |
| D、HClO |
为除去括号内杂质,下列有关试剂和操作方法不正确的是( )
| A、苯(苯酚):稀NaOH溶液,分液 |
| B、乙醇(乙酸):KOH溶液,分液 |
| C、乙烷(乙烯):溴水,洗气 |
| D、苯(溴):稀NaOH溶液,分液 |
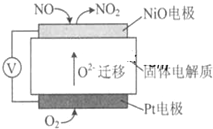 SO2、NOx是大气的主要污染物.
SO2、NOx是大气的主要污染物.