题目内容
下列物质是第三周期元素最高价氧化物对应的水化物(含氧酸),其中酸性就强的是( )
| A、H2SiO3 |
| B、H3PO4 |
| C、H2SO4 |
| D、HClO4 |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:元素的非金属性越强,对应的最高价氧化物对应的水化物的酸性越强,根据同周期元素的非金属性变化规律分析.
解答:
解:元素的非金属性越强,对应的最高价氧化物对应的水化物的酸性越强,同周期元素从左到右非金属性逐渐增强,则Si、P、S、Cl中Cl的非金属性最强,所以酸性最强的是HClO4,
故选D.
故选D.
点评:本题以元素非金属性强弱的判断为载体考查了元素周期律,题目难度不大,注意元素周期律的正确应用.

练习册系列答案
相关题目
如图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( ) 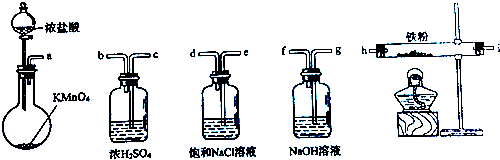

| A、a-b-c-d-e-e-f-g-h |
| B、a-e-d-c-b-h-i-g |
| C、a-d-e-c-b-h-i-g |
| D、a-c-b-d-e-h-i-f |
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
A、异戊二烯( )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 |
| B、邻羟基苯甲酸与NaHCO3溶液反应 |
| C、甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应 |
| D、2-氯丁烷与NaOH乙醇溶液共热发生消去反应 |
下列说法正确的是( )
| A、相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键 |
| B、苯和油脂均不能使酸性高锰酸钾溶液褪色 |
| C、红外光谱分析不能区分乙醇和乙酸乙酯 |
| D、蛋白质溶液中加硫酸铵或氯化铜溶液,均会发生蛋白质的变性 |
下列属于第ⅣA的元素的是( )
| A、C | B、N | C、O | D、S |
下列反应的离子方程式正确的是( )
A、乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+OH-
| ||
B、向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-
| ||
| C、苯酚钠溶液中通入少量二氧化碳:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | ||
D、乙醛溶液与新制氢氧化铜碱性悬浊液共热CH3CHO+2Cu(OH)2+OH-
|
下列各组物质仅用蒸馏水不能鉴别出的是( )
| A、苯、酒精、硝基苯 |
| B、氧化铜、二氧化锰、活性碳 |
| C、食盐、烧碱、硝酸铵 |
| D、蔗糖、硫酸铜粉末、碳酸钙粉末 |
 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A、常压下五种元素的单质中,Z单质的熔点最高 |
| B、Z2水溶液中通入YO2后褪色,表现了YO2的漂白性 |
| C、工业上合成X的氢化物采用高温高压催化剂条件 |
| D、Y、Z的阴离子电子层结构都与R原子的相同 |