题目内容
某研究性学习小组讨论下列四种装置的有关用法,其中不合理的是( )
A、 此装置:可用来证明碳的非金属性比硅强 |
B、 此装置:橡皮管的作用是平衡压强,使水顺利流下 |
C、 此装置:用图示的方法能检查此装置的气密性 |
D、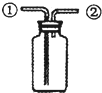 此装置:可收集二氧化碳或氨气 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.碳酸的酸性大于硅酸;
B.橡皮管可使下部的压力转移到上方;
C.液柱法测定装置的气密性,甲、乙中应出现液面差;
D.①进气可收集二氧化碳,②进气可收集氨气.
B.橡皮管可使下部的压力转移到上方;
C.液柱法测定装置的气密性,甲、乙中应出现液面差;
D.①进气可收集二氧化碳,②进气可收集氨气.
解答:
解:A.发生二氧化碳与硅酸钠的反应,生成硅酸和碳酸钠,碳酸的酸性大于硅酸,可比较非金属性C>Si,故A正确;
B.橡皮管可使下部的压力转移到上方,从而利用压强平衡的原理使液体顺利流下,故B正确;
C.液柱法测定装置的气密性,甲、乙中应出现液面差,而图中甲、乙液面相平,不能检查气密性,故C错误;
D.二氧化碳的密度比空气大,氨气的密度比空气的小,则①进气可收集二氧化碳,②进气可收集氨气,故D正确;
故选C.
B.橡皮管可使下部的压力转移到上方,从而利用压强平衡的原理使液体顺利流下,故B正确;
C.液柱法测定装置的气密性,甲、乙中应出现液面差,而图中甲、乙液面相平,不能检查气密性,故C错误;
D.二氧化碳的密度比空气大,氨气的密度比空气的小,则①进气可收集二氧化碳,②进气可收集氨气,故D正确;
故选C.
点评:本题考查化学实验方案的评价,涉及非金属性与酸性的比较、装置气密性的检查、气体的收集及装置的作用,综合性较强,侧重实验原理和物质性质的考查,选项B为解答的难点,题目难度不大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
下列叙述中,正确的是( )
| A、2.4克金属镁变成镁离子时失去的电子数目为0.1NA(NA代表阿伏加德罗常数) |
| B、40g NaOH溶解于500mL水中,所得溶液的物质的量浓度为2mol?L-1 |
| C、1mol H2的质量是2g?mol-1 |
| D、等物质的量的O3和H2O中所含的原子个数相等 |
设nA为阿佛加德罗常数的值,下列说法正确的是( )
| A、常温下,23gNO2含有nA个氧原子 |
| B、1molFe与足量的稀HNO3反应转移2nA个电子 |
| C、常温常压下,22.4LCCl4含有nA个CCl4分子 |
| D、1molFe2+与 足量H2O2溶液反应,转移2nA个电子 |
下列物质间的转化只有加入酸才能一步实现的是( )
| A、Zn→ZnSO4 |
| B、CuO→CuCl2 |
| C、CaCO3→CO2 |
| D、BaCl2→BaSO4 |
下列说法不正确的是( )
| A、金属单质与盐溶液的反应都是置换反应 |
| B、4Fe(OH)2+O2+2H2O=4Fe(OH)3属于化合反应 |
| C、SO2+Cl2+2H2O=2HCl+H2SO4属于氧化还原反应 |
| D、AgNO3+HCl=AgCl↓+HNO3该反应不能说明盐酸酸性比硝酸强 |

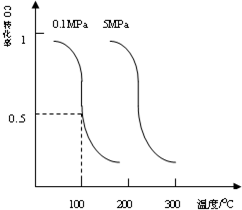 研究和开发CO2和CO的创新利用是环境保护和资源利用的双赢的课题.
研究和开发CO2和CO的创新利用是环境保护和资源利用的双赢的课题. 某学生用电子天平和必要的化学实验仪器测定铁铝合金中各组分含量,其实验装置如图所示:实验时,取一块铁铝合金,将其切成碎块后全部加入到盛有50mL 5.0mol?L-1 NaOH溶液的烧杯中.试回答下列问题:
某学生用电子天平和必要的化学实验仪器测定铁铝合金中各组分含量,其实验装置如图所示:实验时,取一块铁铝合金,将其切成碎块后全部加入到盛有50mL 5.0mol?L-1 NaOH溶液的烧杯中.试回答下列问题: