题目内容
19.下列反应可以表示如图的能量变化的是( )
| A. | Al和Fe2O3的铝热反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | NaOH溶液与CH3COOH溶液反应 | D. | 甲烷在O2中的燃烧反应 |
分析 生成物具有的总能量高于反应物具有的总能量,该反应为吸热反应.
①放热反应:有热量放出的化学反应,因为反应物具有的总能量高于生成物具有的总能量.常见放热反应:燃烧与缓慢氧化,中和反应;金属与酸反应制取氢气,生石灰和水反应,铝热反应等.
②吸热反应:有热量吸收的化学反应,因为反应物具有的总能量低于生成物具有的总能量.常见的吸热反应:C(s)+H2O(g)→CO(g)+H2O; C+CO2→CO的反应,Ba(OH)2•8H2O与NH4Cl的反应,以及KClO3、KMnO4、CaCO3的分解等.
解答 解:A.Al和Fe2O3的铝热反应是放热反应,故A错误;
B.Ba(OH)2•8H2O与NH4Cl的反应是吸热反应,故B正确;
C.NaOH溶液与CH3COOH溶液的中和反应是放热反应,故C错误;
D.甲烷在O2中的燃烧反应是放热反应,故D错误;
故选B.
点评 本题考查化学反应的热量变化,难度不大,学生应注重归纳中学化学中常见的吸热或放热的反应,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.有机物X的分子数为C6H10O2,在稀硫酸中加热可得到Y、Z两种物质,其中Y能使溴的CCl4溶液褪色,能与NaHCO3溶液反应且分子中只含有一个甲基,则X最多有(不考虑立体异构)( )
| A. | 7种 | B. | 6种 | C. | 5种 | D. | 4种 |
10.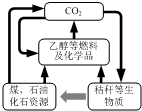 我国《可再生能源法》倡导碳资源的高效转化及循环利用(如图所示).下列做法与上述理念相违背的是( )
我国《可再生能源法》倡导碳资源的高效转化及循环利用(如图所示).下列做法与上述理念相违背的是( )
 我国《可再生能源法》倡导碳资源的高效转化及循环利用(如图所示).下列做法与上述理念相违背的是( )
我国《可再生能源法》倡导碳资源的高效转化及循环利用(如图所示).下列做法与上述理念相违背的是( )| A. | 大力发展煤的气化及液化技术 | B. | 加快石油等化石燃料的开采和使用 | ||
| C. | 以CO2 为原料生产可降解塑料 | D. | 将秸秆进行加工转化为乙醇燃料 |
7.下列能说明氯元素比硫元素非金属性强的是( )
①HCl比H2S稳定;②HClO4酸性比H2SO4强;③Cl2能与H2S反应生成S;④Cl原子最外层有7个电子,S原子最外层有6个电子;⑤Cl2比S更易与H2化合生成相应气态氢化物;⑥盐酸是强酸,而氢硫酸是弱酸.
①HCl比H2S稳定;②HClO4酸性比H2SO4强;③Cl2能与H2S反应生成S;④Cl原子最外层有7个电子,S原子最外层有6个电子;⑤Cl2比S更易与H2化合生成相应气态氢化物;⑥盐酸是强酸,而氢硫酸是弱酸.
| A. | ①②③④⑤⑥ | B. | ①②③④⑥ | C. | ①②③⑤ | D. | ②④⑥ |
14.已知(NH4)2SO4在高温下分解,产物是SO2、H2O、N2和NH3.有关该反应的下列说法正确的是( )
| A. | N2既是氧化产物又是还原产物 | |
| B. | NH4+部分被氧化 | |
| C. | 氧化产物和还原产物的物质的量比为3:1 | |
| D. | 氧化产物和还原产物的物质的量比为1:4 |
11.对下图的实验装置和操作评价不合理的是( )


| 选项 | 装置和操作 | 评价 |
| A | 用装置①量取15.00ml的NaOH溶液 | 错误:不能用酸式滴定管,应改用碱式滴定管 |
| B | 用装置②制备Cl2 | 错误:氯气密度大于空气,收集时导管应长进短出 |
| C | 用装置③验证溴乙烷发生消去反应生成烯烃 | 正确:生成的乙烯可使高锰酸钾褪色 |
| D | 关闭活塞a,从b处加水,以检查装置④的气密性 | 正确:b处加水后,左右液面形成稳定的高度差,证明气密性良好 |
| A. | A | B. | B | C. | C | D. | D |
8.25℃时,将a mol/L的氨水与0.01mol/L的HCl溶液等体积混合,反应后溶液的pH=10,下列说法正确的是(忽略溶液混合后体积的变化)( )
| A. | 此时溶液中NH3•H2O的物质的量浓度为$\frac{a-0.01}{2}$+10-10-10-4mol/L | |
| B. | 溶液中c(NH4+)=c(Cl-) | |
| C. | 此时水的电离程度最大 | |
| D. | 25℃时NH3•H2O的电离平衡常数Kb=$\frac{{{{10}^{-9}}}}{a-0.01}$(mol/L) |
