题目内容
13.1个氧原子的质量是2.657×10-26kg,则32kgO2中所含O2的数目最接近于( )| A. | 3.01×1023 | B. | 5.32×1026 | C. | 6.02×1026 | D. | 1.2×1026 |
分析 氧气分子由氧原子构成,则32g氧气中氧原子总质量为32kg,结合氧原子质量计算氧原子数目,而每个氧气分子含有2个氧原子,则氧气分子数目为氧原子的$\frac{1}{2}$.
解答 解:1个氧原子的质量是2.657×10-26kg,则32kgO2中含有氧原子数目为$\frac{32}{2.657×1{0}^{-26}}$,而每个氧气分子含有2个氧原子,则氧气分子数目为$\frac{32}{2.657×1{0}^{-26}}$×$\frac{1}{2}$=6.02×1026,故选C.
点评 本题考查微粒数目计算,比较基础,旨在考查学生对基础知识的理解掌握.

练习册系列答案
相关题目
3.化学与社会、生活密切相关.对下列现象或事实的解释不正确的是( )
| A. | 二氧化硅用途广泛,石英、水晶、光导纤维的主要成分都是二氧化硅 | |
| B. | 碘是人体必需微量元素,日常生活中食用的加碘盐中添加的是碘单质 | |
| C. | 漂白粉既可作棉、麻、纸张的漂白剂,又可作游泳池的消毒剂 | |
| D. | 燃煤时加入适量石灰石,可减少废气中SO2的量 |
4.M、N、X、Y四种物质之间有如下转化关系(反应条件和其它产物已略去).下列选项不符合的是( )
M$→_{反应①}^{+X}$N$→_{反应②}^{+X}$Y.
M$→_{反应①}^{+X}$N$→_{反应②}^{+X}$Y.
| A. | M:N2 X:O2 | B. | M:HNO3 X:Fe | C. | M:S X:O2 | D. | M:NO X:O2 |
1.已知a g气体A与b g气体B的物质的量相同,则下列说法中错误的( )
| A. | A与B两种气体的相对分子质量之比为a:b | |
| B. | 同质量的A、B两种气体分子数之比为b:a | |
| C. | 同温同压时,两种气体A与B的密度之比为a:b | |
| D. | 同温同体积时,同质量的A、B两种气体的压强之比为a:b |
2.下列分散系最不稳定的是( )
| A. | 向CuSO4溶液中加入NaOH溶液得到的分散系 | |
| B. | 向水中加入食盐得到的分散系 | |
| C. | 向沸水中滴入饱和FeCl3溶液得到的红褐色液体 | |
| D. | 向NaOH溶液中通入CO2得到的无色溶液 |
15.水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸和甲醇在酸性催化剂下合成水杨酸( )甲酯并计算其产率.实验步骤如下:
)甲酯并计算其产率.实验步骤如下:
Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,以及约10mL甲苯(甲苯与 水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯5.3g.
常用物理常数如下:
请根据以上信息回答下列问题:
(1)仪器A的名称是冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)实验中加入沸石的作用是防暴沸;
(3)加入甲苯的作用是将反应产生的水从反应体系中分离出来,使合成水杨酸甲酯反应的化学平衡向右移动,从而提高反应的产率.
(4)反应结束后,分离甲醇所采用操作的名称是蒸馏.
(5)洗涤操作中,前后两次水洗的目的分别是为了洗掉洗掉大部分硫酸和洗掉碳酸氢钠.
(6)在蒸馏操作中,仪器选择及安装都正确的是(填标号)b.

(7)本实验的产率为70%(保留两位有效数字).
 )甲酯并计算其产率.实验步骤如下:
)甲酯并计算其产率.实验步骤如下:Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,以及约10mL甲苯(甲苯与
 水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯5.3g.
常用物理常数如下:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)实验中加入沸石的作用是防暴沸;
(3)加入甲苯的作用是将反应产生的水从反应体系中分离出来,使合成水杨酸甲酯反应的化学平衡向右移动,从而提高反应的产率.
(4)反应结束后,分离甲醇所采用操作的名称是蒸馏.
(5)洗涤操作中,前后两次水洗的目的分别是为了洗掉洗掉大部分硫酸和洗掉碳酸氢钠.
(6)在蒸馏操作中,仪器选择及安装都正确的是(填标号)b.

(7)本实验的产率为70%(保留两位有效数字).

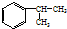 ,A的含有苯环的同分异构体(除A外)有7种,其中核磁共振氢谱显示为2组峰,且峰面积比为3:1的同分异构体是
,A的含有苯环的同分异构体(除A外)有7种,其中核磁共振氢谱显示为2组峰,且峰面积比为3:1的同分异构体是 (写结构简式).
(写结构简式). +nHCHO$→_{△}^{催化剂}$
+nHCHO$→_{△}^{催化剂}$ +nH2O.
+nH2O. G:
G: .
.