题目内容
固体NH4Br置于密闭容器中,某温度下发生反应:NH4Br(s)?NH3(g)+HBr(g),2HBr(g)?Br2(g)+H2(g),2min后测知H2的浓度为0.5mol?L-1,HBr的浓度为4mol?L-1,若上述反应速率用v(NH3)表示,则下列速率正确的是( )
| A、0.5mol?L-1?min-1 |
| B、2.5mol?L-1?min-1 |
| C、2mol?L-1?min-1 |
| D、1.25mol?L-1?min-1 |
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:根据可逆反应:NH4Br(s)?NH3(g)+HBr(g),2HBr(g)?Br2(g)+H2(g),溴化铵分解生成的氨气浓度与溴化氢浓度相等,根据2min后的氢气浓度和溴化氢浓度可以计算出溴化铵分解生成的溴化氢浓度,就可以知道生成的氨气的浓度,最后根据v=
计算出氨气的反应速率.
| △c |
| △t |
解答:
解:根据反应可知,溴化铵分解生成的氨气浓度与溴化氢浓度相等,溴化铵分解生成的溴化氢的浓度为:c(HBr)+2c(H2)=4mol/L+2×0.5mol/L=5mol/L,所以2min后溴化铵分解生成的氨气的浓度为:c(NH3)=c总(HBr)=5mol/L,
氨气的平均反应速率为:
=2.5 mol/(L?min),
故选B.
氨气的平均反应速率为:
| 5mol/L |
| 2min |
故选B.
点评:本题考查了化学反应速率的计算,题目难度中等,解题关键是分析、理解题中可逆反应中氨气与溴化氢的浓度关系,根据2min后氢气和溴化氢的浓度计算出氨气的浓度,试题充分考查了学生的分析、理解信息能力及灵活应用所学知识解决实际问题的能力.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
升高温度时,化学反应速率加快,主要原因是( )
| A、该化学反应的过程是吸热的 |
| B、该化学反应的过程是放热的 |
| C、反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| D、分子运动速率加快,使该反应物分子的碰撞机会增多 |
水中加入下列溶液对水的电离平衡不产生影响的是( )
| A、NaHSO4溶液 |
| B、NaOH溶液 |
| C、KAl(SO4)2溶液 |
| D、KI溶液 |
在一个容积为2L的密闭容器中,发生如下反应:3X(气)+Y(气)═2Z(气),若最初加入的X、Y和Z都是1mol,反应中X的平均反应速率为0.12mol?L-1?s-1.若要产物Z为1.8mol,反应所需的时间为( )
| A、5s | B、10s |
| C、15s | D、20s |
下列有关金属腐蚀与防护的说法正确的是( )
A、金属被腐蚀的本质是:M+nH2O=M(OH)n+
| ||
| B、当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | ||
| C、在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | ||
| D、可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
下列烧杯中盛放的都是稀H2SO4,在Cu电极上产生大量气泡的是( )
A、 |
B、 |
C、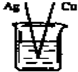 |
D、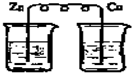 |
下列说法中正确的是( )
| A、丙烯分子中有8个σ键,1个π键 |
| B、在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C、NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力 |
| D、NCl3和BC13分子中,中心原子都采用sp3杂化 |
下列离子方程式正确的是( )
| A、氢氧化镁中滴加盐酸:H++OH-═H2O |
| B、在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C、已知电离平衡常数:H2CO3>HClO>HCO3-,向次氯酸钠溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- |
| D、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+NH3?H2O+2BaSO4↓ |