题目内容
升高温度时,化学反应速率加快,主要原因是( )
| A、该化学反应的过程是吸热的 |
| B、该化学反应的过程是放热的 |
| C、反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| D、分子运动速率加快,使该反应物分子的碰撞机会增多 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:升高温度能加快反应速率的主要原因是活化分子的百分数增加,以此解答该题.
解答:
解:升高温度,分子能量增加,增加了活化分子的百分数,增加有效碰撞的次数,反应速率增大,与反应为吸热、放热无关,
故选C.
故选C.
点评:本题考查化学反应速率的影响,为高考高频考点,侧重于学生的基础知识的考查,有利于夯实双基,培养学生的学习积极性,难度不大.

练习册系列答案
相关题目
室温时,下列各组离子在指定溶液中可以大量共存的是( )
| A、1.0mol/L的K2S溶液:Cl-,Fe3+,Na+,SO42- | ||
| B、加入甲基橙试液呈红色的溶液:NH4+,Fe2+,SO42-,NO3- | ||
C、室温下,
| ||
| D、饱和氯水中:NO3-,Na+,SO32-,Cl- |
在25℃时,某溶液中由水电离出的c(H+)=1×10-12 mol/L,则该溶液的pH可能为( )
| A、10 | B、7 | C、6 | D、2 |
下列关于合金的说法不正确的是( )
| A、合金的熔点一般比它的成分金属的熔点高 |
| B、合金的硬度一般比它的成分金属大 |
| C、合金与各成分金属相比,具有许多优良的物理、化学或机械的性能 |
| D、合金在工业上的用途比纯金属更广 |
下列有关物质性质的应用正确的是( )
| A、二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
| B、液氨汽化时要吸收大量的热,可用作制冷剂 |
| C、生石灰能与水反应,可用来干燥氯气 |
| D、氯化铝是一种电解质,可用于电解法制铝 |
固体NH4Br置于密闭容器中,某温度下发生反应:NH4Br(s)?NH3(g)+HBr(g),2HBr(g)?Br2(g)+H2(g),2min后测知H2的浓度为0.5mol?L-1,HBr的浓度为4mol?L-1,若上述反应速率用v(NH3)表示,则下列速率正确的是( )
| A、0.5mol?L-1?min-1 |
| B、2.5mol?L-1?min-1 |
| C、2mol?L-1?min-1 |
| D、1.25mol?L-1?min-1 |
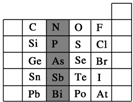 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.