题目内容
13.A、B两原子,A原子L层比B原子M层少3个电子,B原子L层电子数恰为A原子L层电子数的2倍,则A、B分别是( )| A. | 硅和钠 | B. | 硼和氮 | C. | 碳和氯 | D. | 碳和铝 |
分析 A原子L层比B原子M层少3个电子,说明A为第二周期元素,B为第三周期元素,B原子L层电子数恰为A原子L层电子数的2倍,说明A的L层电子数为4,B的M电子数为7,以此解答.
解答 解:A原子L层比B原子M层少3个电子,说明A为第二周期元素,B为第三周期元素,B原子L层电子数恰为A原子L层电子数的2倍,说明A的L层电子数为4,B的M电子数为7,
则A为C元素,Bi为Cl元素.
故选C.
点评 本题考查核外电子排布规律、原子结构与位置关系等,为高频考点,侧重于学生的分析能力的考查,难度不大,理解核外电子排布规律并能灵活运用.

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
3.常温下能用铁制容器盛放的是( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 硫酸铜 | D. | 稀硫酸 |
18.下列环境问题与CO2有关的是( )
| A. | 臭氧空洞 | B. | 酸雨 | C. | 光化学烟雾 | D. | 温室效应 |
5.下列物质在水中的电离方程式错误的是( )
| A. | MgSO4=Mg2++SO42- | B. | Ba(OH)2=Ba2++OH2- | ||
| C. | NaHCO3=Na++HCO3- | D. | H2SO4=2H++SO42- |
2.写出下列除杂的离子方程式,括号内的物质为杂质.
| 物质(杂质) | 离子方程式 |
| FeCl2 (FeCl3) | (1)2Fe3++Fe=3Fe2+ |
| CO2 (HC1) | (2)H++HCO3-=H2O+CO2↑ |
| NaHC03 溶液(Na2C03) | (3)CO32-+CO2+H2O=2HCO3- |
3.分子式为C4H7Cl的链状有机物的同分异构体(不考虑顺反异构)有( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |




 以香豆素3甲酸乙酯(
以香豆素3甲酸乙酯(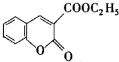 )为原料合成香豆素3甲酸(
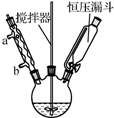
)为原料合成香豆素3甲酸(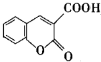 )的装置如图所示,实验步骤如下:
)的装置如图所示,实验步骤如下: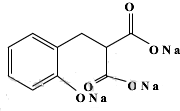 +C2H5OH+H2O.
+C2H5OH+H2O.