题目内容
下列说法正确的是( )
| A、脂肪烃、芳香烃和卤代烃都属于烃 |
| B、天然气、沼气和水煤气都属于可再生的清洁能源 |
| C、工业上分别用热还原法、加热法和电解法冶炼镁、铝和铜 |
| D、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
考点:电解质与非电解质,清洁能源,强电解质和弱电解质的概念,金属冶炼的一般原理,饱和烃与不饱和烃
专题:物质的分类专题
分析:A、根据烃是指仅含有碳氢两种元素的化合物;
B、根据煤、石油和天然气属于化石燃料,是不可再生能源;
C、根据金属的活动性强弱选择合适的冶炼方法,一般来说,活泼金属用电解法,较活泼金属用热还原法,不活泼金属如Hg、Ag等用热分解法冶炼;
D、根据非电解质、强电解质以及弱电解质的概念;
B、根据煤、石油和天然气属于化石燃料,是不可再生能源;
C、根据金属的活动性强弱选择合适的冶炼方法,一般来说,活泼金属用电解法,较活泼金属用热还原法,不活泼金属如Hg、Ag等用热分解法冶炼;
D、根据非电解质、强电解质以及弱电解质的概念;
解答:
解:A、卤代烃中含有卤素原子,不属于烃,故A错误;
B、天然气属于不可再生的清洁能源,故B错误;
C、铜用热还原法冶炼,镁、铝用电解法冶炼,故C错误;
D、蔗糖在水溶液中或熔融状态下均不导电属于非电解质;硫酸钡在溶液中完全电离属于强电解质;水能够发生部分电离属于弱电解质,故D正确;
故选D.
B、天然气属于不可再生的清洁能源,故B错误;
C、铜用热还原法冶炼,镁、铝用电解法冶炼,故C错误;
D、蔗糖在水溶液中或熔融状态下均不导电属于非电解质;硫酸钡在溶液中完全电离属于强电解质;水能够发生部分电离属于弱电解质,故D正确;
故选D.
点评:本题主要考查了烃的概念、可再生资源、金属的冶炼、电解质等,难度中等,注意概念的掌握.

练习册系列答案
相关题目
下列说法正确的是( )
| A、SO2和CO2是造成“酸雨”的罪魁祸首 |
| B、“水华”是由于水中富含氯元素造成的 |
| C、“光化学烟雾”与NO2的排放有关 |
| D、燃烧树叶和氢气都不会造成大气污染 |
下列实验操作中正确的是( )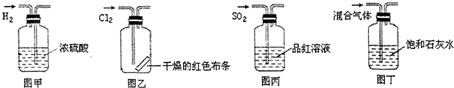

| A、图甲所示,可得到干燥的氢气 |
| B、图乙所示,可以验证氯气的漂白性 |
| C、图丙所示,可以验证SO2的漂白性 |
| D、图丁所示,若石灰水变浑浊,证明混合气体中一定含有CO2 |
分别取pH=2的两种一元酸HX和HY的溶液各50mL,加入过量的镁粉,充分反应后,收集H2的体积在相同状况下分别为V1和V2,若V1>V2,下列说法正确的是( )
| A、HX一定是弱酸 |
| B、NaX水溶液的碱性弱于NaY水溶液的碱性 |
| C、HX一定是强酸 |
| D、反应过程中二者生成H2的速率相同 |
下列反应一定需要加氧化剂才能发生的是( )
| A、NO2→NO3- |
| B、SO2→SO3 |
| C、Cl2→NaClO |
| D、Fe3+→Fe2+ |
下列离子方程式的书写正确是( )
| A、实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O |
| B、铁和稀盐酸反应:Fe+2H+=H2↑+Fe2+ |
| C、氢氧化钡溶液与稀H2SO4 反应:Ba2++SO42-=BaSO4↓ |
| D、钠投入水中:Na+H2O=Na++OH-+H2↑ |
 X、Y、Z、W四种常见化合物,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去):
X、Y、Z、W四种常见化合物,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去):