题目内容
下列反应一定需要加氧化剂才能发生的是( )
| A、NO2→NO3- |
| B、SO2→SO3 |
| C、Cl2→NaClO |
| D、Fe3+→Fe2+ |
考点:氧化还原反应
专题:氧化还原反应专题
分析:一定需要加入氧化剂才能完成,则选项中物质具有还原性,加入氧化剂之后还原剂所含元素的化合价升高.
解答:
解:A.N元素化合价降升高,可加入氧化剂或与水反应自身发生氧化还原反应生成,故A错误;
B.S元素化合价升高,被氧化,应加入氧化剂才能实现,故B正确;
C.Cl元素化合价升高,无需加入氧化剂,氯气与氢氧化钠溶液反应可生成,故C错误;
D.Fe元素化合价降低,被还原,可加入还原剂实现,故D错误.
故选B.
B.S元素化合价升高,被氧化,应加入氧化剂才能实现,故B正确;
C.Cl元素化合价升高,无需加入氧化剂,氯气与氢氧化钠溶液反应可生成,故C错误;
D.Fe元素化合价降低,被还原,可加入还原剂实现,故D错误.
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中的元素化合价变化为解答的关键,侧重还原剂发生氧化反应的考查,选项A、C为解答的易错点,题目难度不大.

练习册系列答案
相关题目
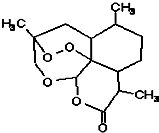 中国国家主席胡锦涛在中非合作论坛北京峰会上承诺:“提供3亿元人民币无偿援款帮助非洲防治疟疾,用于提供青蒿素药品及设立30个抗疟中心”.中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )
中国国家主席胡锦涛在中非合作论坛北京峰会上承诺:“提供3亿元人民币无偿援款帮助非洲防治疟疾,用于提供青蒿素药品及设立30个抗疟中心”.中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )| A、是一种烃 |
| B、属于高分子化合物 |
| C、属于芳香族化合物 |
| D、分子式是C15H22O5 |
下列说法正确的是( )
| A、脂肪烃、芳香烃和卤代烃都属于烃 |
| B、天然气、沼气和水煤气都属于可再生的清洁能源 |
| C、工业上分别用热还原法、加热法和电解法冶炼镁、铝和铜 |
| D、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
 如图是向100mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图.根据图所得结论正确的是( )
如图是向100mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图.根据图所得结论正确的是( )| A、原来盐酸的物质的量浓度为1 mol?L-1 |
| B、x处为含NaOH0.1 mol的溶液 |
| C、原来盐酸的物质的量浓度为0.1 mol?L-1 |
| D、x处为含NaOH0.001 mol的溶液 |
下列几组物质中,属于同分异构体的一组是( )
A、 与 与  |
B、 与 与 |
| C、CH3CH2OH与CH3OCH3 |
D、CH3CH2OH与 |
中科大教授钱逸泰等以CCl4和金属钠为原料,在700°C时反应制造出纳米级金刚石粉末和另一种化合物.同学们对此有下列一些“理解”,你认为其中错误的是( )
| A、金刚石属于金属单质 |
| B、制造过程中元素种类没有改变 |
| C、CCl4是一种化合物 |
| D、这个反应是置换反应 |
物质的量浓度相等的三种溶液:①H2CO3 ②NaOH ③Na2CO3溶液,下列说法不正确的是( )
| A、水电离出的c(H+):③>①>② |
| B、溶液的pH:②>③>① |
| C、①和②等体积混合后的溶液:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
| D、①和③等体积混合后的溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
