题目内容
2.物质的性质决定其用途,下列应用中利用了物质氧化性的是( )| A. | 氧化铝做耐火材料 | B. | 纯碱去油污 | ||
| C. | 食醋除水垢 | D. | 漂白粉漂白织物 |
分析 利用了物质氧化性,则发生氧化还原反应,且物质中元素的化合价降低,以此来解答.
解答 解:A.氧化铝熔点高,用于耐火材料属于物理性质,故A错误;
B.纯碱水解呈碱性,有利于油脂的水解,没有发生化学变化,故B错误;
C.醋酸与水垢(碳酸钙、氢氧化镁)发生复分解反应,故C错误;
D.漂白粉有效成分为次氯酸钙,具有强氧化性,可用于漂白,故D正确.
故选D.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应、反应中元素的化合价变化是解答本题的关键,侧重化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学生学习的积极性,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.在100mL 1mol•L-1的纯碱溶液中,不断搅拌并逐滴加入240mL 0.5mol•L-1盐酸,完全反应后在标准状况下生成CO2的体积为( )
| A. | 44 8mL | B. | 224 mL | C. | 336mL | D. | 0 mL |
13.下列各化合物的命名中正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. |  2-甲基丁烷 2-甲基丁烷 | ||
| C. |  甲基苯酚 甲基苯酚 | D. |  3-丁醇 3-丁醇 |
10.下列反应过程中的能量变化情况符合如图的是( )


| A. | NaOH与H2SO4发生中和反应 | B. | 氧化钙和水反应 | ||
| C. | NH4Cl和Ba(OH)2•8H2O的反应 | D. | 一氧化碳气体的燃烧 |
7.在0.2mol•L-1Cu(NO3)2和Fe(NO3)3溶液中,通入一定量H2S气体,下列不可能发生的离子方程式是( )
| A. | H2S+2Fe3+→S↓+2Fe2++2H+ | B. | H2S+Fe2+→2H++FeS↓ | ||
| C. | H2S+Cu2+→CuS↓+2H+ | D. | 2H++2NO3-+3H2S→2NO↑+3S↓+4H2O |
11.常温下,有关 0.1mol/L NH4Cl 溶液(pH<7),下列说法不正确的是( )
| A. | 根据以上信息,可推断NH3•H2O为弱电解质 | |
| B. | 加水稀释过程中,c(H+)•c(OH-) 的值增大 | |
| C. | 加入K2CO3固体可促进 NH4+的水解 | |
| D. | 同pH的NH4Cl溶液和CH3COOH溶液,由水电离出的c(H+) 前者大 |
12.某有机物A的红外光谱和核磁共振氢谱图如图所示,下列说法中错误的是( )
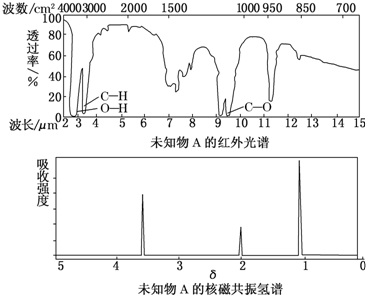

| A. | 由红外光谱可知,该有机物中至少有三种不同的化学键 | |
| B. | 若A的化学式为C2H6O,则其结构简式为CH3-O-CH3 | |
| C. | 仅由其核磁共振氢谱图无法得知其分子中的氢原子总数 | |
| D. | 由核磁共振氢谱图可知,该有机物分子中有三种不同的氢原子 |
 下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质.气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质.气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫 .
.