题目内容
17. 下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质.气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质.气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫色(部分反应物和生成物及溶剂水已略去).
请回答下列问题:
(1)D的化学式为KCl.
(2)C的电子式为
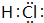 .
.(3)写出A溶液和甲反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(4)写出工业上制备B的化学方程式:N2+3H2$?_{催化剂}^{高温高压}$2NH3.
分析 乙、丙、丁为单质,一定条件下乙与丙反应得到B,丙、丁在点燃条件下反应得到C,且B与C相遇生成大量白烟生成E,可知B为NH3,C为HCl,则丙为H2,乙为N2,丁为Cl2,E为NH4Cl,NH4Cl与强碱A反应生成NH3与D,且D的焰色为紫色,含有K元素,故A为KOH、D为KCl,甲是日常生活中常见的金属,能与KOH反应生成氢气,则甲为Al,据此解答.
解答 解:乙、丙、丁为单质,一定条件下乙与丙反应得到B,丙、丁在点燃条件下反应得到C,且B与C相遇生成大量白烟生成E,可知B为NH3,C为HCl,则丙为H2,乙为N2,丁为Cl2,E为NH4Cl,NH4Cl与强碱A反应生成NH3与D,且D的焰色为紫色,含有K元素,故A为KOH、D为KCl,甲是日常生活中常见的金属,能与KOH反应生成氢气,则甲为Al.
(1)D的化学式为KCl,故答案为:KCl;
(2)C为HCl,电子式为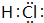 ,故答案为:
,故答案为: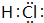 ;
;
(3)A溶液和甲反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)工业上制备NH3的化学方程式:N2+3H2$?_{催化剂}^{高温高压}$2NH3,故答案为:N2+3H2$?_{催化剂}^{高温高压}$2NH3.
点评 本题考查无机物的推断,反应现象及焰色反应等时推断的突破口,再结合转化关系中特殊反应进行推断,难度不大,注意对基础知识的掌握.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
12.下列说法中正确的是( )
| A. | 用铁与稀硝酸反应来制备氢气 | |
| B. | 氨气、液氨和氨水是同一种物质 | |
| C. | NO2溶于水发生了氧化还原反应,它既是氧化剂又是还原剂 | |
| D. | 钠在氧气中燃烧发出白光,生成白色固体氧化钠 |
8.下列说法正确的是( )
| A. | 乙烯能使溴水、酸性高锰酸钾溶液褪色,其反应类型相同 | |
| B. | 某烷烃R的相对分子质量为86,其氯代物只有2种,则R的名称一定为2,3-二甲基丁烷 | |
| C. | 若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物只有CHCl3 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
5.用如图所示装置能达到有关实验目的是( )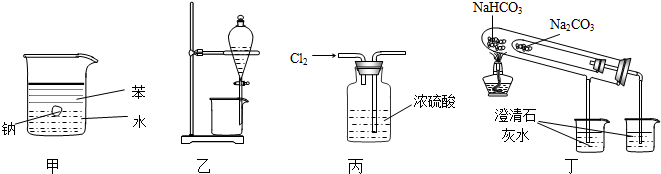

| A. | 用甲图装置证明密度ρ(苯)<ρ(钠)<ρ(水) | |
| B. | 用乙图装置分离酒精和四氯化碳 | |
| C. | 用丙图装置干燥Cl2 | |
| D. | 用丁图装置比较NaHCO3和Na2CO3的热稳定性 |
12.下列反应的离子方程式书写正确的是( )
| A. | 硫酸和氯氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | 碳酸钠与盐酸反应:Na2CO3+2H+═2Na++CO2↑+H2O | |
| C. | Ca(NO3)2溶液和Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 铁钉放入硫酸铁溶液中:Fe+Fe3+═2Fe2+ |
2.物质的性质决定其用途,下列应用中利用了物质氧化性的是( )
| A. | 氧化铝做耐火材料 | B. | 纯碱去油污 | ||
| C. | 食醋除水垢 | D. | 漂白粉漂白织物 |
9.将5.6gFe投入浓硝酸中,产生红棕色气体A,把所得溶液减压蒸干,得到20gFe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红棕色的Fe2O3和气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的体积为( )
| A. | 1120mL | B. | 2240mL | C. | 3360mL | D. | 4480mL |
6.下列解释事实的离子方程式正确的是( )
| A. | 明矾做净水剂:Al3++3H2O═Al (OH)3↓+3H+ | |
| B. | 小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 漂白液加白醋,提高漂白效率:CH3COOH+ClO-═HClO+CH3COO- | |
| D. | 酸化的淀粉碘化钾溶液在空气中放置一段时间变蓝:4I-+O2+2H2O═2I2+4OH- |
7.下列物质与常用危险化学品的分类不对应的是( )
| A. | Na--遇湿易燃物品 | B. | Na2O2-是氧化剂 | ||
| C. | 浓硫酸-易爆品 | D. | KOH-腐蚀品 |