题目内容
将0.1mol/L的下列物质的水溶液,从常温加热到80℃(不计水的蒸发),溶液的pH不变的是
A.NaCl B.(NH4)2SO4 C.Ba(OH)2 D.H2SO4
D
【解析】
试题解析:升高温度时氯化钠中性溶液中的水的离子积变大,氢离子的浓度变大,故溶液的pH变小,故A错误;升高温度促进水解,氢离子浓度越大,PH变小,故B错误;升高温度时氢氧化钡溶液中氢氧根离子的浓度不变,但升高温度时水的离子积变大,则氢离子的浓度变大,故溶液的pH变小,故C错误;升高温度时硫酸中的氢离子浓度不变,则溶液的pH不变,故D正确。
考点:弱电解质在水溶液中的电离平衡、影响盐类水解程度的主要因素

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 H2CO3 B.OH-+HS-
H2CO3 B.OH-+HS- 、
、 、
、 、
、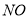 、
、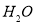 。则该反应中还原产物是______ ;若反应过程中转移了0.3
。则该反应中还原产物是______ ;若反应过程中转移了0.3 电子,则氧化产物的质量_____
电子,则氧化产物的质量_____ 。
。 Al(OH)4― + H+ ;②NH3+H2O
Al(OH)4― + H+ ;②NH3+H2O