题目内容
20.下列溶液中,c(Cl-)与50mL 1mol/L的AlCl3溶液中c(Cl-)相等的是( )| A. | 150mL 1 mol/L的NaCl溶液 | B. | 75mL 2 mol/L的NH4Cl溶液 | ||
| C. | 150mL 3 mol/L的KCl溶液 | D. | 75mL 1 mol/L的BaCl2溶液 |
分析 根据离子的物质的量浓度=溶质的物质的量浓度×一个溶质分子中含有的离子的个数,与溶液的体积无关.
解答 解:50mL 1mol/L的AlCl3溶液中c(Cl-)=1mol/L×3=3mol/L,
A、150mL 1mol/L的NaCl溶液中c(Cl-)=1mol/L×1=1mol/L,故A错误;
B、75mL 2mol/L的NH4Cl溶液中c(Cl-)=2mol/L×1=2mol/L,故B错误;
C、150mL 3mol/L的KCl溶液中c(Cl-)=3mol/L×1=3mol/L,故C正确;
D、75mL 1mol/L的BaCl2溶液中c(Cl-)=1mol/L×2=2mol/L,故D错误;
故选C.
点评 本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
5.在通常情况下,稀有气体很难与其他元素发生化学反应,其原因是( )
| A. | 稀有气体最外层电子数均为8个,很稳定 | |
| B. | 稀有气体的电子层数比较多,很稳定 | |
| C. | 稀有气体的最外层电子数均达到稳定结构 | |
| D. | 稀有气体的原子核所带电荷较多 |
4.在密闭容器中进行反应N2(g)+3H2(g)?2NH3(g);△H=-akJ/mol.N2、H2起始的物质的量分别为10mol和30mol,达到平衡时H2的转化率为25%.并放出热量bkJ若从NH3开始在相同条件下欲使平衡时各成分的百分含量与前者相同,则其NH3的转化率和吸收的热量为( )
| A. | 25%和7.5akJ | B. | 25%和3bkJ | C. | 75%和(a-b) kJ | D. | 75%和(10a-b) kJ |
5.检验居室中有甲醛气体,可连续多次抽取居室空气样品,注入到少量(1~2mL)低浓度(1×10-4mol/L)的酸性高锰酸钾溶液中.据此,下列说法正确的是( )
| A. | 说明甲醛是具有氧化性的气体 | B. | 反应中甲醛被还原 | ||
| C. | 最终酸性高锰酸钾溶液是红色 | D. | 最终酸性高锰酸钾溶液是无色 |

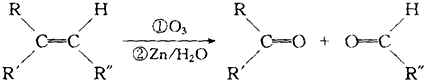
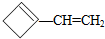
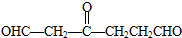 ,则该烯烃的结构不可能是( )
,则该烯烃的结构不可能是( )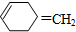
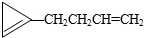
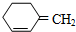

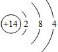 .D燃烧放出大量热量,有望成为二十一世纪的新能源,与“传统能源”相比,它具有便于储运,比较安全(写出两点)等更加优越的特点.
.D燃烧放出大量热量,有望成为二十一世纪的新能源,与“传统能源”相比,它具有便于储运,比较安全(写出两点)等更加优越的特点.